Dorzolamide
Renseignements généraux
Impuretés du dorzolamide et dorzolamide
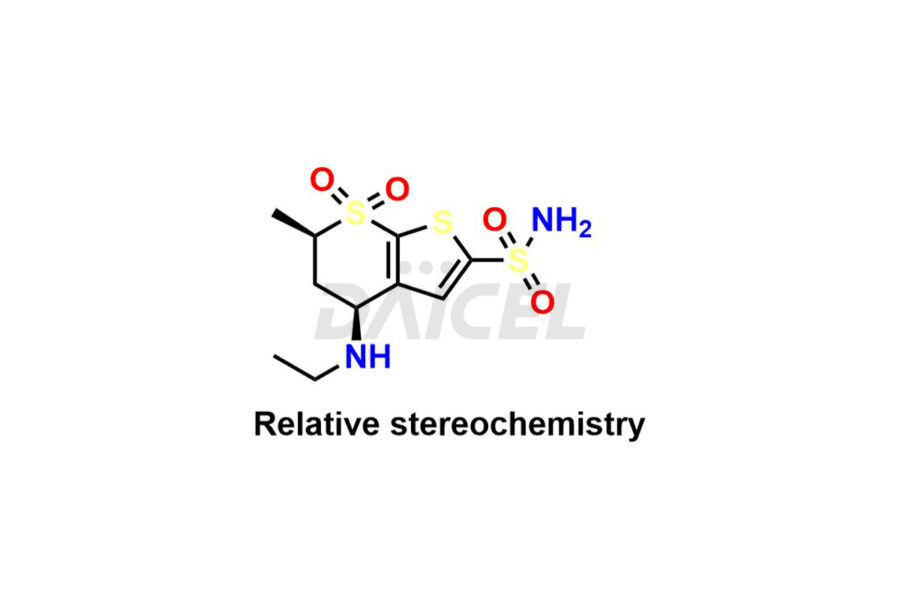
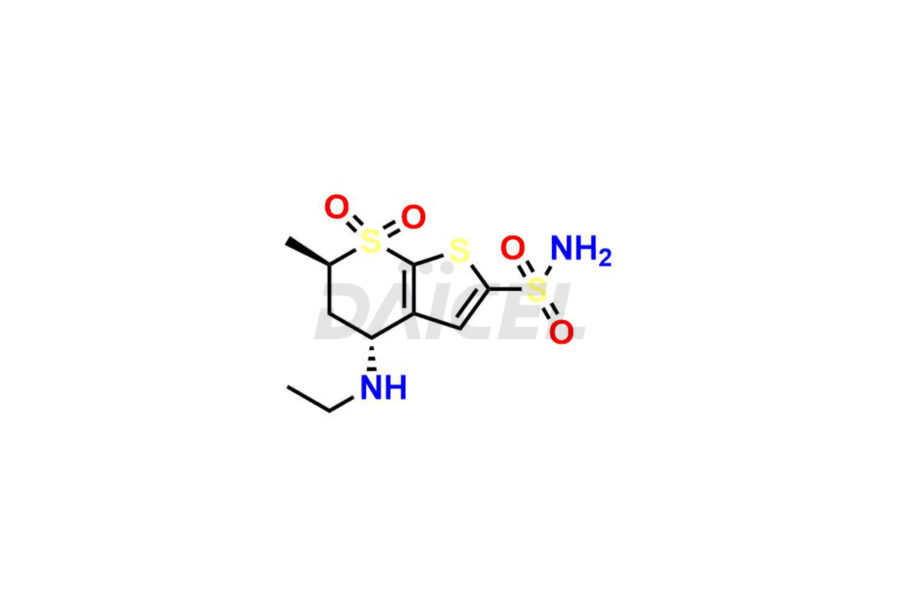
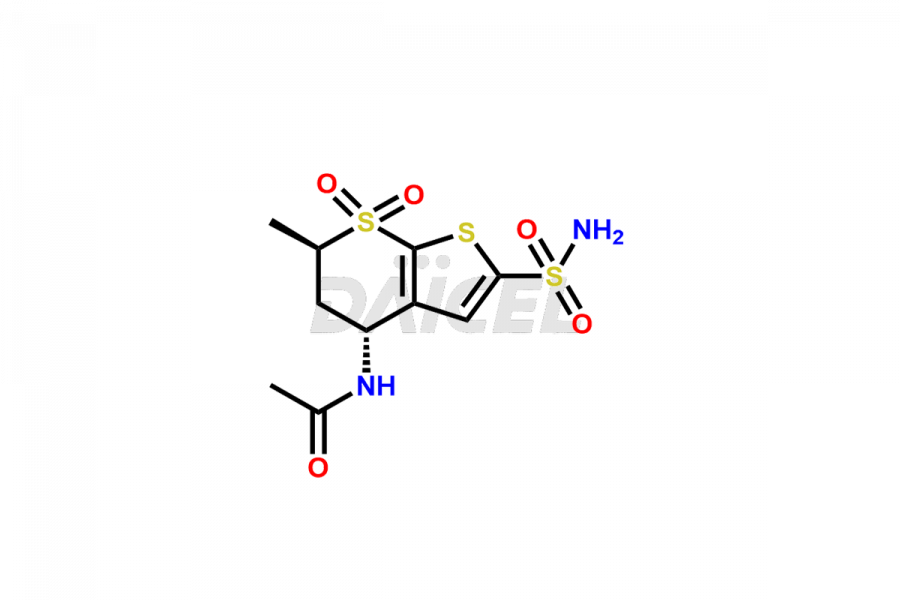
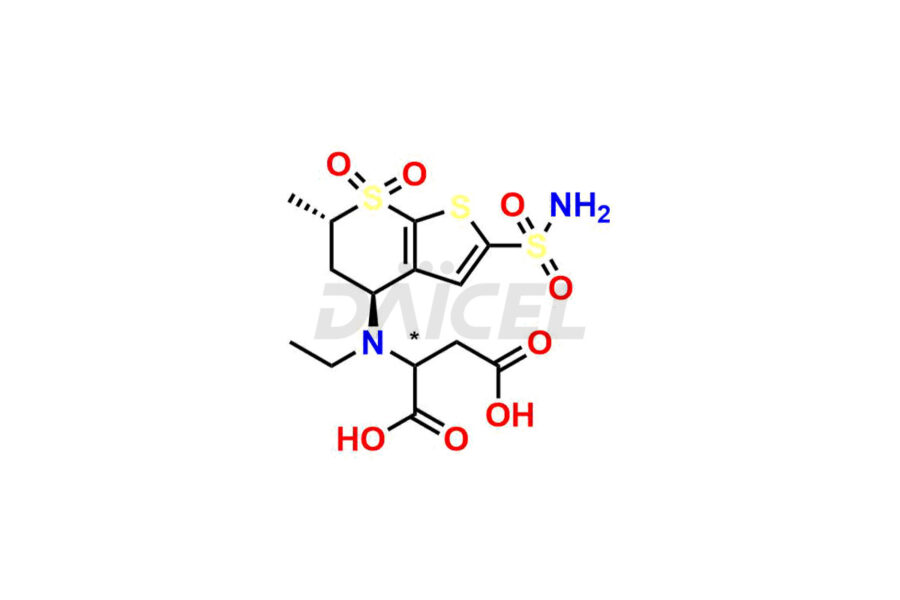
Daicel Pharma se spécialise dans l'offre d'impuretés de haute qualité pour le dorzolamide, un ingrédient pharmaceutique actif. Ces impuretés, notamment les diastéréomères du dorzolamide, l'énantiomère du dorzolamide, les diastéréomères intermédiaires du dorzolamide, l'énantiomère intermédiaire du dorzolamide, l'adduit à l'acide maléique du dorzolamide et l'analogue du dorzolamide N-déséthyl-N-acétyle, jouent un rôle essentiel dans l'évaluation de la pureté, de la fiabilité et de la sécurité du dorzolamide. Daicel Pharma propose également une synthèse personnalisée d'impuretés de dorzolamide pour répondre aux exigences des clients, avec des options de livraison disponibles dans le monde entier.
Dorzolamide [CAS : 120279/96/1] est un médicament antiglaucomateux qui agit comme un inhibiteur de l'anhydrase carbonique. Il abaisse la pression intraoculaire dans le traitement du glaucome à angle ouvert. De plus, le dorzolamide sert d’agent antihypertenseur.
Dorzolamide : utilisation et disponibilité commerciale
Le dorzolamide, disponible sous Trusopt, est un inhibiteur de deuxième génération de l'anhydrase carbonique II qui traite le glaucome. Le dorzolamide abaisse la pression intraoculaire en réduisant la production d'humeur aqueuse. Il est formulé sous forme de collyre à 2 % et réduit efficacement la pression intraoculaire (PIO). Les patients atteints de glaucome à angle ouvert ou d'hypertension oculaire peuvent bénéficier des effets réduisant la PIO du dorzolamide.
Structure du dorzolamide et mécanisme d’action 
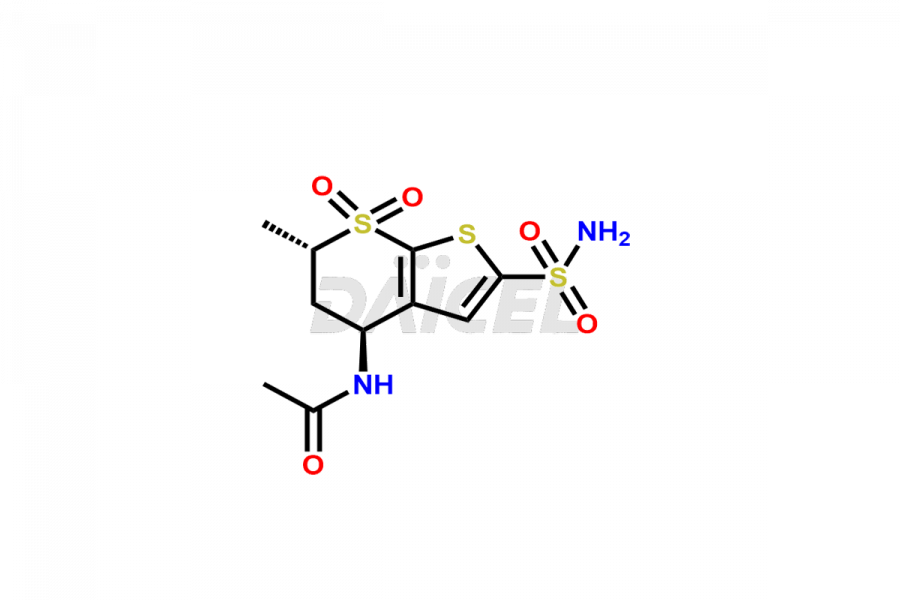
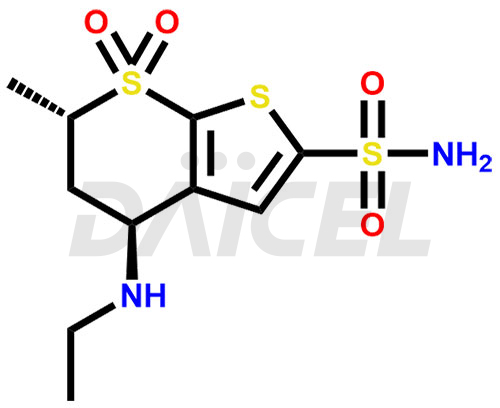
Le nom chimique du dorzolamide est (4S,6S)-4-(éthylamino)-5,6-dihydro-6-méthyl-4H-thiéno-[2,3-b]thiopyran-2-sulfonamide 7,7-dioxyde. Sa formule chimique est C10H16N2O4S3, et son poids moléculaire est d'environ 324.4 g/mol.
Le dorzolamide inhibe l'anhydrase carbonique II humaine dans les processus ciliaires de l'œil et diminue la sécrétion d'humeur aqueuse.
Impuretés et synthèse du dorzolamide
La formation d'impuretés dans le Dorzolamide peut avoir un impact sur sa qualité, sa sécurité et son efficacité. Des impuretés peuvent apparaître pendant le processus de synthèse1 ou le stockage du dorzolamide et peut inclure des produits de dégradation, des solvants résiduels ou des substances associées. Il est nécessaire de synthétiser et de caractériser ces impuretés pour comprendre leur nature et leur impact potentiel. Les méthodes analytiques, telles que la chromatographie et la spectroscopie, aident à analyser et à quantifier les impuretés du dorzolamide. La mise en œuvre de mesures de contrôle strictes permet d'établir des limites acceptables pour les niveaux d'impuretés, garantissant ainsi la qualité et la pureté du dorzolamide pour une utilisation sûre et efficace chez les patients atteints de glaucome.
Daicel Pharma propose un certificat d'analyse (CoA) complet pour les étalons d'impuretés du dorzolamide, y compris les diastéréomères du dorzolamide, l'énantiomère du dorzolamide, les diastéréomères intermédiaires du dorzolamide, l'énantiomère intermédiaire du dorzolamide, l'adduit de l'acide maléique du dorzolamide et l'analogue du dorzolamide N-déséthyl-N-acétyle. Ils sont générés à partir d’une installation d’analyse conforme aux normes cGMP. Le CoA fournit un rapport de caractérisation détaillé avec des données obtenues grâce à des techniques telles que la RMN 1H, la RMN 13C, l'IR, la MASS et l'analyse de pureté HPLC.2. Nous fournissons des données supplémentaires comme 13C-DEPT sur demande. Daicel Pharma synthétise des impuretés ou des produits de dégradation inconnus du dorzolamide. Chaque livraison dispose d'un rapport de caractérisation complet.
Bibliographie
FAQ
Bibliographie
- Baldwin, John J. ; Ponticello, Gérald S. ; Christy, Marcia E., Dérivés antiglaucoma thiéno-thiopyrane et thiéno-thiépine sulfonamide, compositions et procédé d'utilisation de ceux-ci, Merck and Co., Inc., États-Unis, US4677115A, 30 juin 1987.
- Constance, ML ; Chávez, CM ; Matuszewski, BK, Détermination de faibles niveaux de dorzolamide et de son métabolite dééthylé dans le plasma humain par chromatographie liquide avec spectrométrie de masse en tandem à ionisation chimique à pression atmosphérique, Journal of Pharmaceutical and Biomedical Analysis, Volume : 15, Numéro : 7, Pages : 1001-1008 , 1997
Foire aux Questions
Les impuretés du dorzolamide peuvent-elles être éliminées ou réduites pendant le processus de fabrication ?
Des efforts sont faits pendant le processus de fabrication du Dorzolamide pour minimiser la formation d'impuretés. Des techniques telles que la purification, la filtration et l'optimisation des conditions de réaction aident à éliminer ou à réduire les impuretés. De plus, des pratiques de stockage et d'emballage appropriées peuvent maintenir la qualité du médicament et minimiser la formation d'impuretés.
Y a-t-il des impuretés spécifiques dans le Dorzolamide ?
Les impuretés courantes du dorzolamide comprennent des composés apparentés formés au cours du processus de synthèse, des produits de dégradation résultant de l'exposition à la lumière, à la chaleur ou à l'humidité, ainsi que des solvants résiduels utilisés dans la fabrication.
Quel solvant aide à l’analyse des impuretés du Dorzolamide ?
Le méthanol est un solvant utilisé pour analyser de nombreuses impuretés du dorzolamide.
Quelles sont les conditions de température nécessaires pour stocker les impuretés du Dorzolamide ?
Les impuretés du dorzolamide sont conservées à une température ambiante contrôlée entre 2 et 8 °C ou comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.