Dolutégravir
Renseignements généraux
Impuretés du dolutégravir et dolutégravir
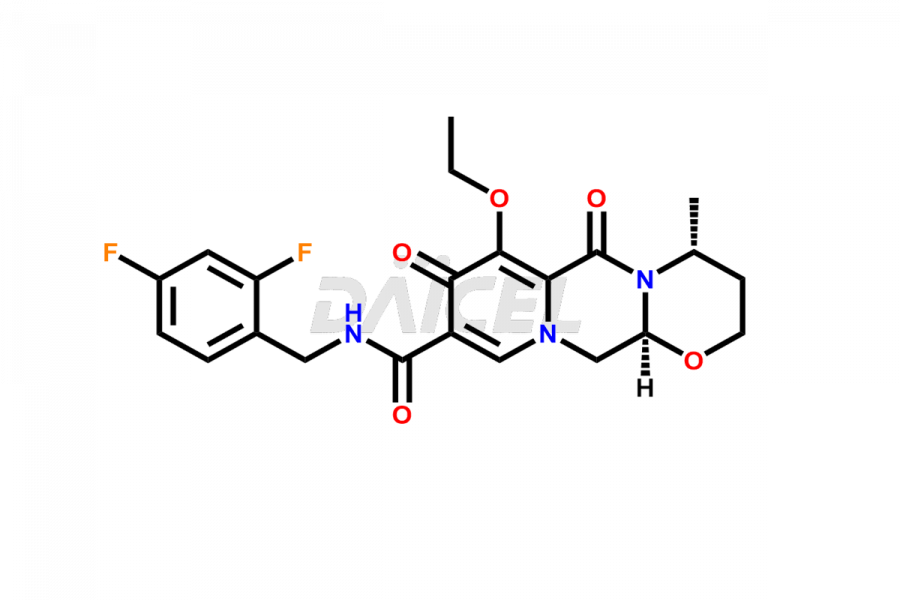
Daicel Pharma se spécialise dans l'offre d'impuretés de haute qualité pour le dolutégravir, un ingrédient pharmaceutique actif. Ces impureté L'isomère O éthyl Dolutegravir et O-Méthyl Dolutegravir jouent un rôle essentiel dans l'évaluation de la pureté, de la fiabilité et de la sécurité du Dolutegravir. Daicel Pharma propose également une synthèse personnalisée des impuretés du dolutégravir pour répondre aux exigences des clients, avec des options de livraison disponibles dans le monde entier.
Dolutégravir [CAS : 1051375/16/6], un inhibiteur de transfert de brin de l'intégrase (INSTI), est un médicament biodisponible par voie orale qui cible l'infection par le VIH-1. Il traite les infections par le VIH avec d'autres agents antirétroviraux.
Dolutégravir : utilisation et disponibilité commerciale
Le dolutégravir est un agent antirétroviral qui traite les infections par le VIH-1. La FDA américaine a approuvé le traitement combiné du dolutégravir et de la [rilpivirine] pour les adultes présentant des taux de virus VIH-1 supprimés et un régime stable pendant au moins six mois. Le dolutégravir est également disponible avec la [lamivudine] et l'[abacavir] pour le traitement du VIH-1 chez les patients adultes et pédiatriques pesant ≥ 10 kg. Le médicament est disponible sous les marques Dovato, Tivicay et Tivicay PD.
Structure et mécanisme d'action du dolutégravir 
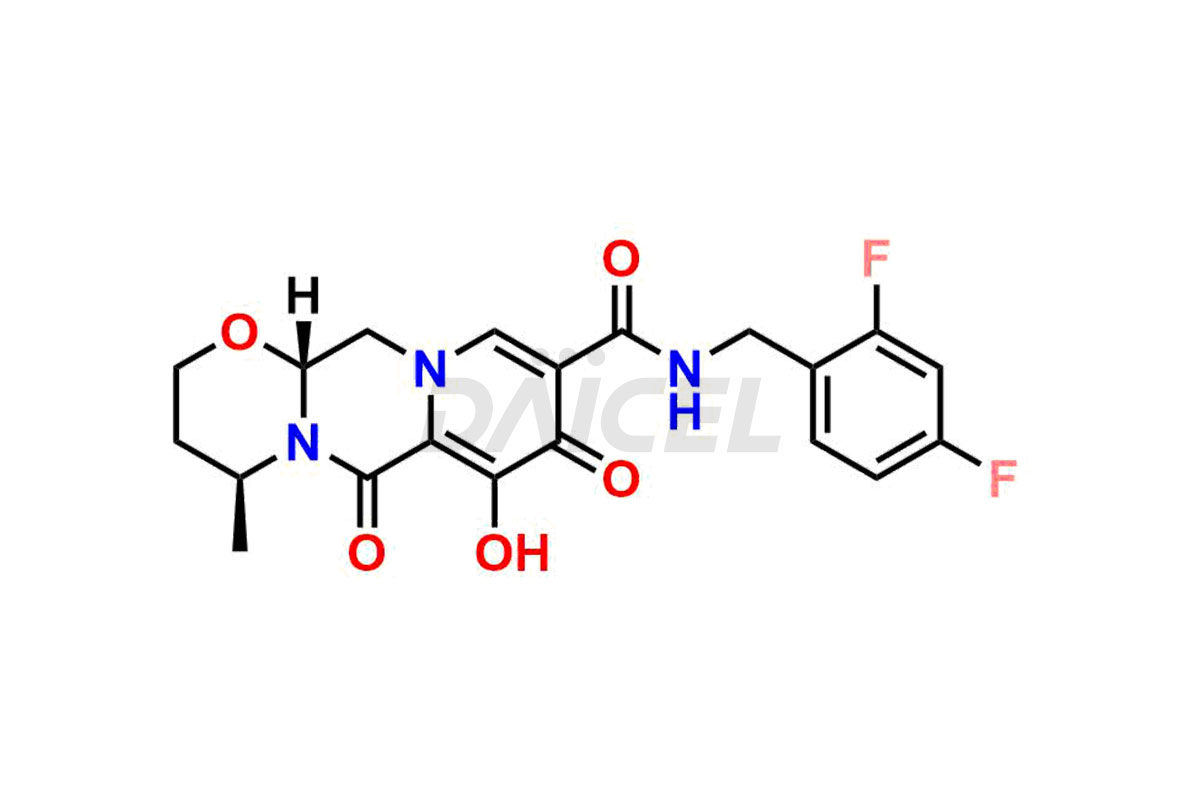
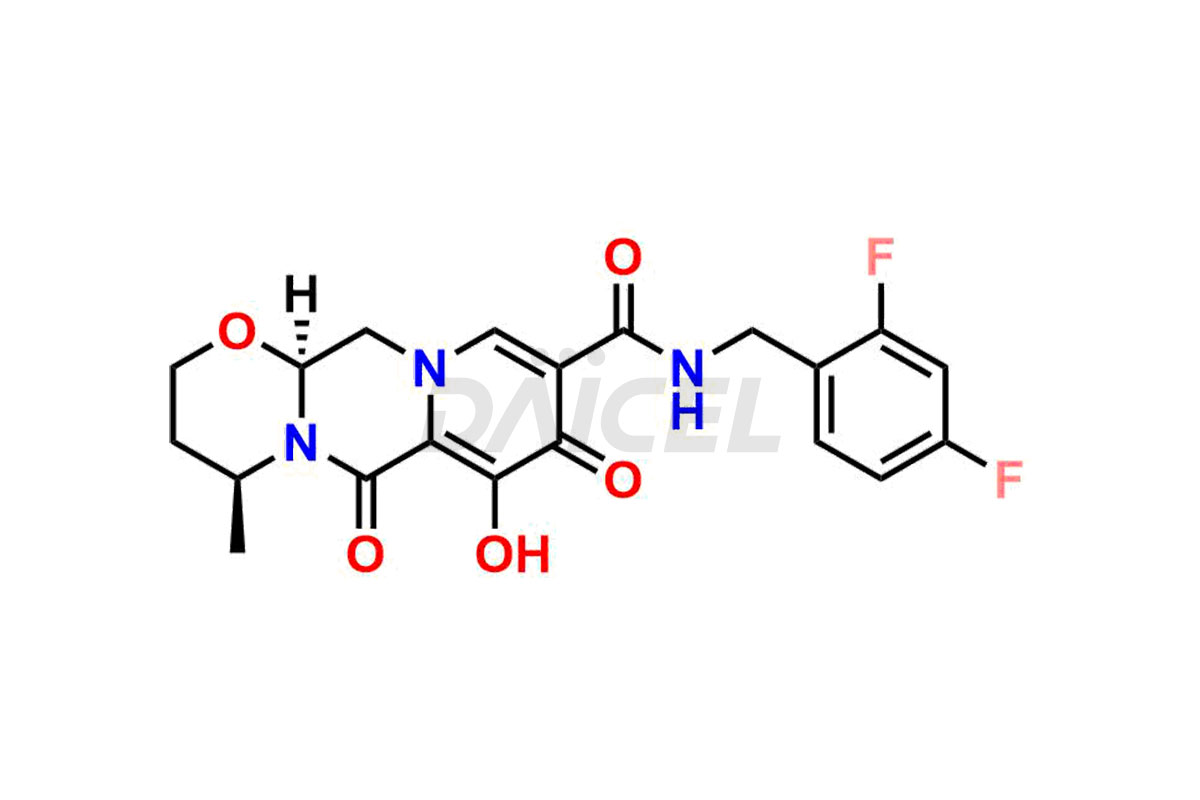
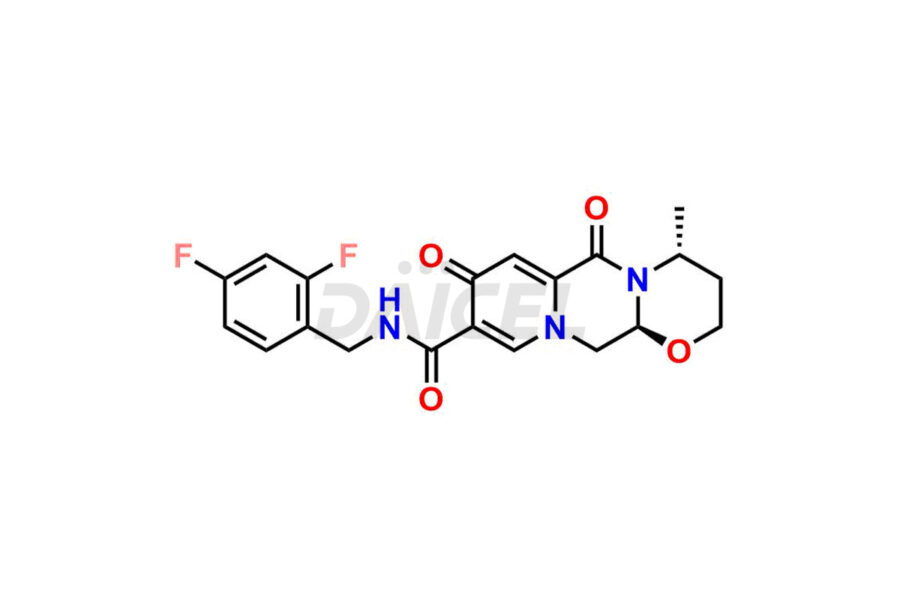
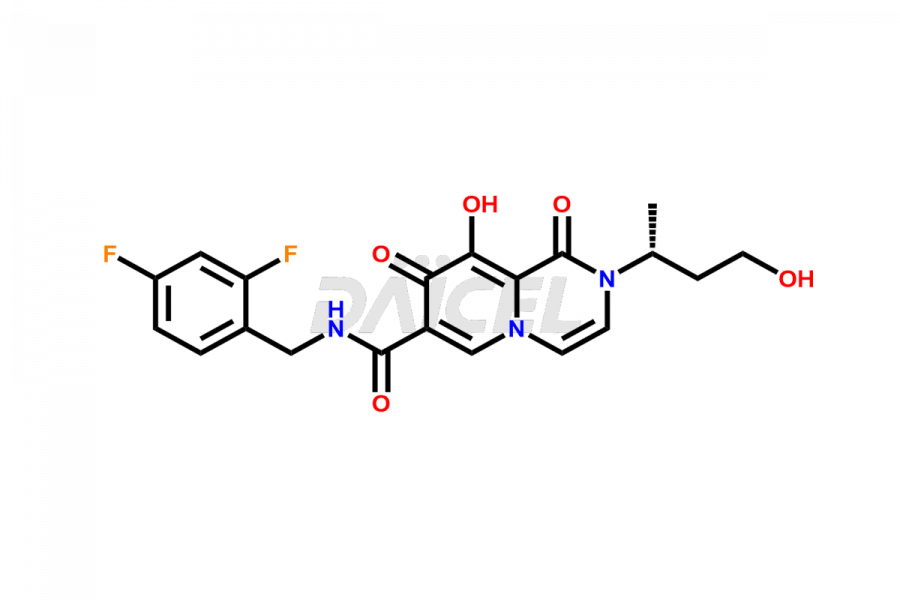
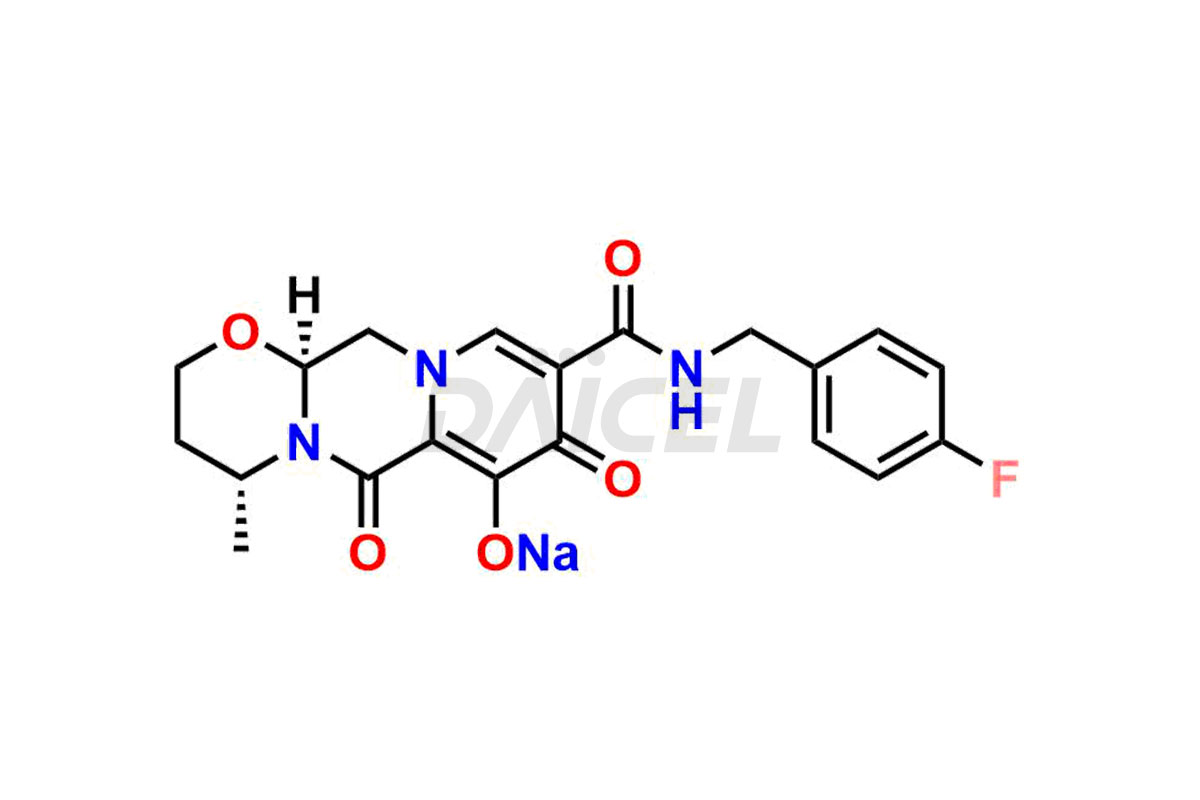
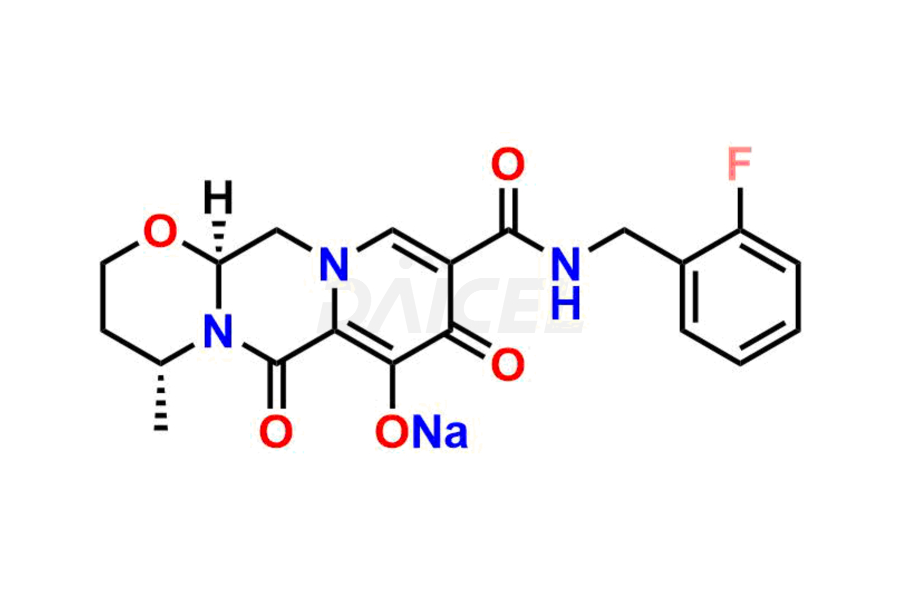
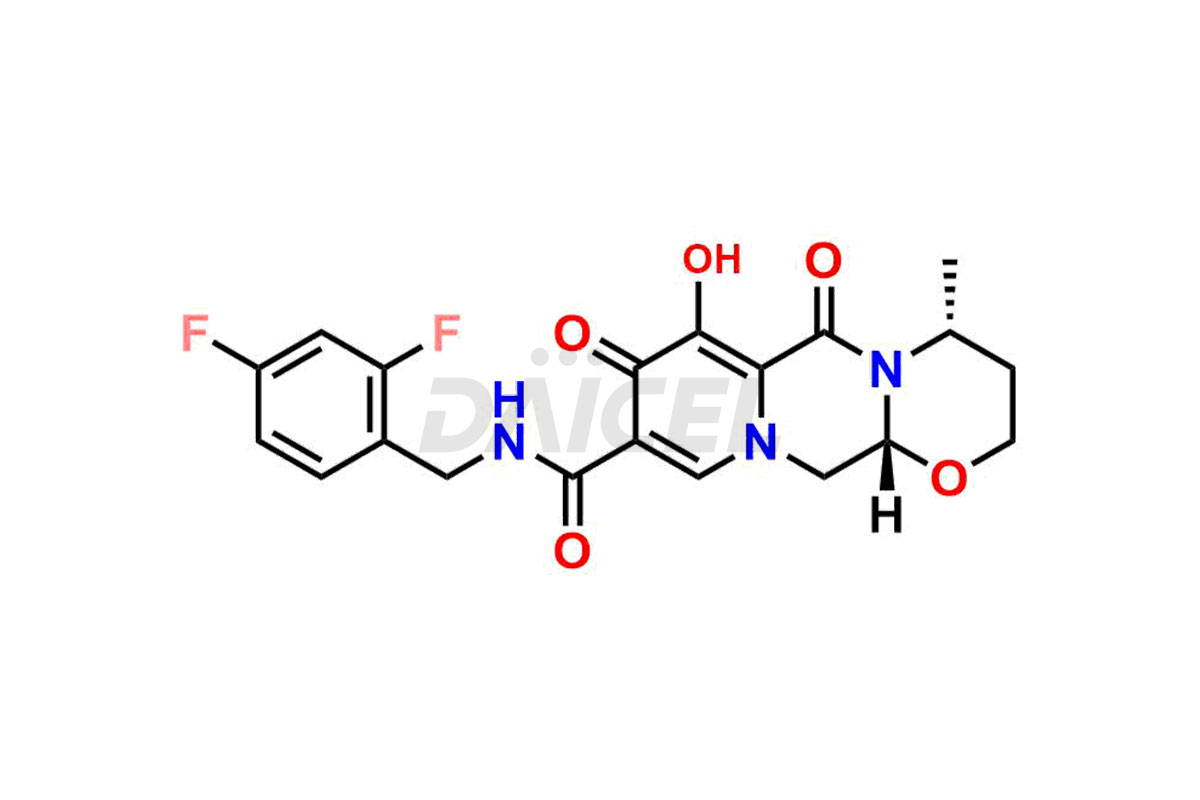
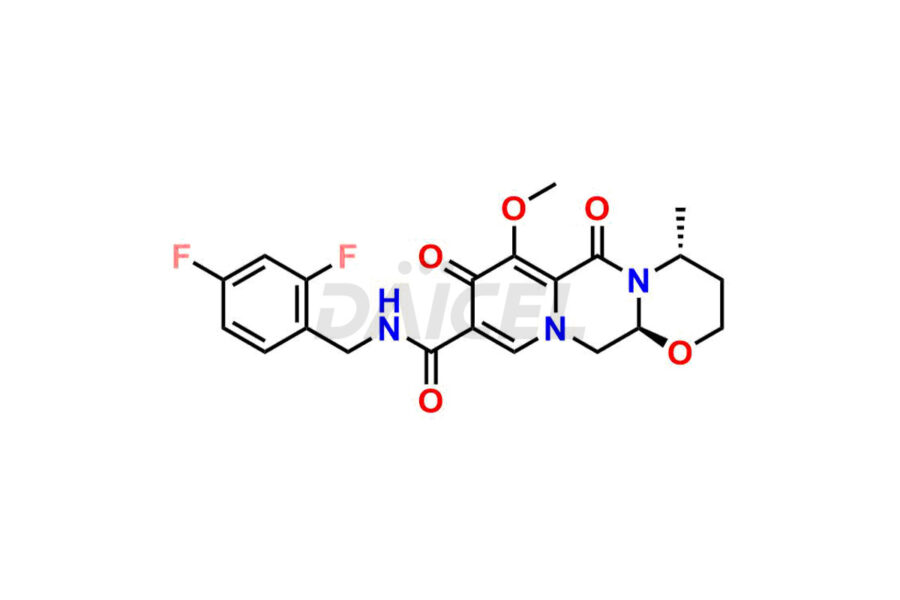
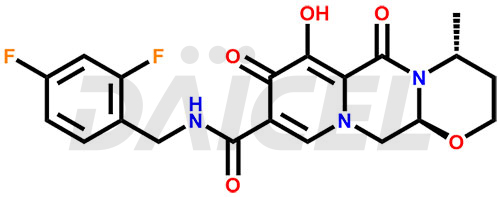
Le nom chimique du dolutégravir est (4R,12aS)-N-[(2,4-Difluorophényl)méthyl]-3,4,6,8,12,12a-hexahydro-7-hydroxy-4-méthyl-6,8. -dioxo-2H-pyrido[1′,2′:4,5]pyrazino[2,1-b][1,3]oxazine-9-carboxamide. Sa formule chimique est C20H19F2N3O5, et son poids moléculaire est d'environ 419.4 g/mol.
Le dolutégravir se lie au site actif de l'intégrase en inhibant l'intégrase du VIH. Il bloque l’étape de transfert de brin de l’intégration de l’acide désoxyribonucléique (ADN) rétroviral et empêche le cycle de réplication du VIH.
Impuretés et synthèse du dolutégravir
La présence d'impuretés dans le dolutégravir, un inhibiteur de transfert de brin de l'intégrase utilisé pour traiter l'infection par le VIH-1, peut affecter sa sécurité, son efficacité et sa stabilité. Des impuretés peuvent apparaître lors de la synthèse1 ou le stockage du dolutégravir et peuvent être liés aux matières premières, aux intermédiaires ou aux produits de dégradation. Il est crucial de synthétiser et d’analyser ces impuretés pour garantir la qualité et la pureté du médicament. Les méthodes analytiques, la chromatographie et la spectroscopie permettront de détecter et de quantifier les impuretés. La mise en œuvre de mesures de contrôle strictes permet d'établir des critères d'acceptation des niveaux d'impuretés, garantissant que le dolutégravir répond aux exigences réglementaires et reste sans danger pour les patients.
Daicel Pharma propose un certificat d'analyse (CoA) complet pour les normes d'impuretés du dolutégravir, notamment l'isomère (S, R)-dolutégravir, l'isomère (S, S)-dolutégravir (impureté dolutégravir-16), des hydroxy dolutégravir, impureté E de dolutégravir et dolutégravir. Impureté-4, Dolutegravir Impureté-5, Dolutegravir R, isomère R, O éthyl Dolutegravir et O-Méthyl Dolutegravir. Ils sont générés à partir d’une installation d’analyse conforme aux normes cGMP. Le CoA fournit un rapport de caractérisation détaillé avec des données obtenues grâce à des techniques telles que la RMN 1H, la RMN 13C, l'IR, la MASS et l'analyse de pureté HPLC.2. Nous fournissons des données supplémentaires comme 13C-DEPT sur demande. Daicel Pharma synthétise des impuretés ou des produits de dégradation inconnus du dolutégravir. Chaque livraison dispose d'un rapport de caractérisation complet.
Bibliographie
FAQ
Bibliographie
- Johns, Brian Alvin ; Kawasuji, Takashi ; Taishi, Teruhiko ; Taoda, Yoshiyuki, Dérivé bicyclique de carbamoylpyridone ayant une activité inhibitrice de l'intégrase du VIH, Shionogi & Co., Ltd., Japon, EP1852434B1, 13 juillet 2011
- Bennetto-Hood, Chantelle; Tabolt, Glenn ; Savine, Paul ; Acosta, Edward P., Une méthode HPLC-MS/MS sensible pour la détermination du dolutégravir dans le plasma humain, Journal of Chromatography B : Analytical Technologies in the Biomedical and Life Sciences, Volume : 945-946, Pages : 225-232, 2014
Foire aux Questions
Quelles méthodes aident à l’analyse des impuretés du dolutégravir ?
Diverses méthodes d'analyse telles que la chromatographie (HPLC, LC), la spectroscopie (UV, IR) et la spectrométrie de masse permettent d'analyser les impuretés du dolutégravir. Ces méthodes permettent de détecter, quantifier et caractériser les impuretés présentes dans la substance médicamenteuse.
Comment les impuretés sont-elles contrôlées lors de la fabrication du dolutégravir ?
Des mesures de contrôle strictes sont mises en œuvre pendant le processus de fabrication du Dolutegravir pour minimiser la formation d'impuretés. Cela comprend l’optimisation des réactions, l’utilisation de matières premières de haute qualité et la mise en œuvre de conditions de stockage et de manipulation appropriées pour éviter la dégradation.
Les impuretés du dolutégravir peuvent-elles affecter la sécurité et l'efficacité du médicament ?
Oui, les impuretés contenues dans le dolutégravir peuvent potentiellement avoir un impact sur sa sécurité et son efficacité. Selon la nature et la concentration des impuretés, elles peuvent introduire une toxicité, réduire la stabilité du médicament ou interférer avec l'action thérapeutique prévue du dolutégravir.
Quelles sont les conditions de température nécessaires pour stocker les impuretés du dolutégravir ?
Les impuretés du dolutégravir sont conservées à une température ambiante contrôlée entre 2 et 8 °C ou comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.