Dexrazoxane
Renseignements généraux
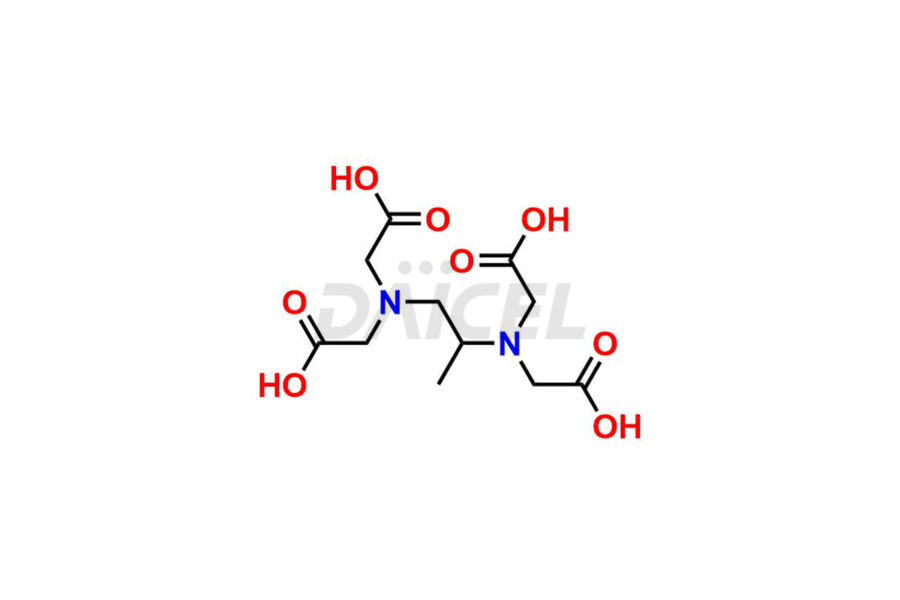
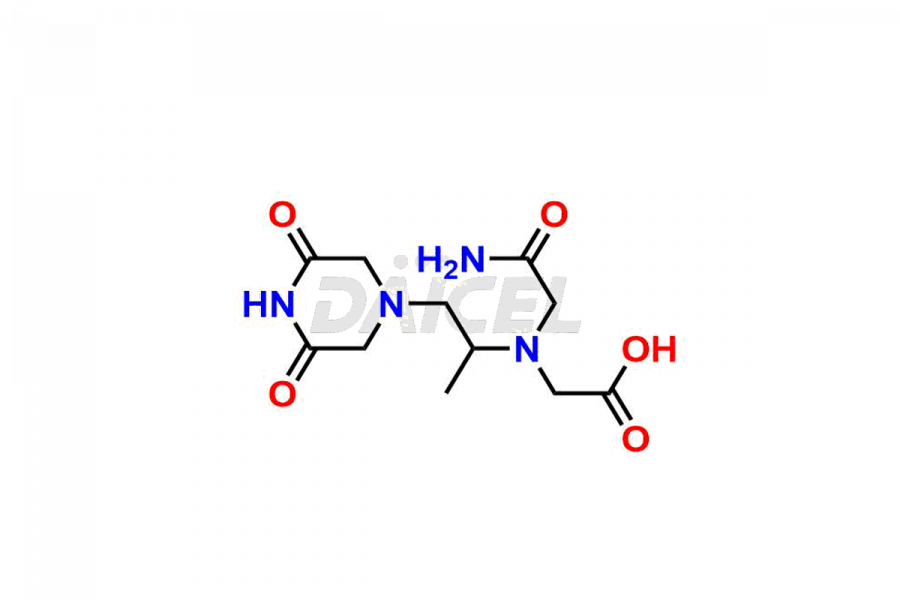
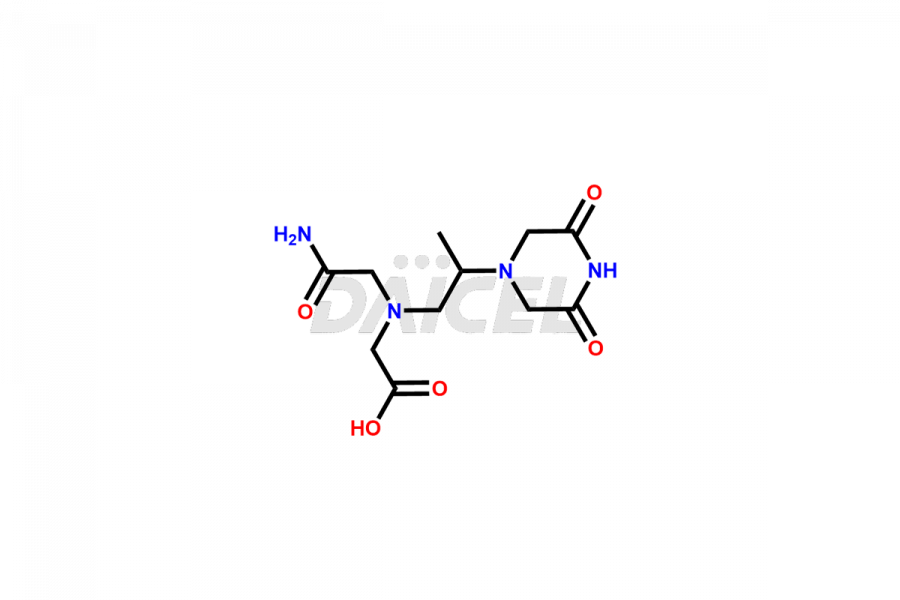
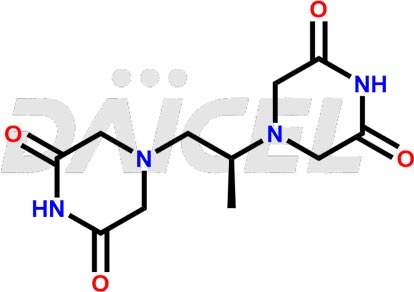
Impuretés de dexrazoxane et dexrazoxane
Daicel Pharma synthétise des impuretés Dexrazoxane d'une qualité exceptionnelle, telles que Dexrazoxane Impurity-A, Dexrazoxane Impurity-C et Dexrazoxane Impurity-D. Ces impuretés sont cruciales pour évaluer la pureté, la fiabilité et la sécurité du Dexrazoxane, un ingrédient pharmaceutique actif. En outre, Daicel Pharma propose une synthèse personnalisée des impuretés du Dexrazoxane pour répondre aux demandes de livraison des clients dans le monde entier.
Dexrazoxane [CAS : 24584/09/6], le (+) -énantiomorphe du razoxane, présente des propriétés chélatrices du fer, chimioprotectrices, cardioprotectrices et antinéoplasiques. Il agit comme un agent antimitotique tout en possédant des effets immunosuppresseurs. Le dexrazoxane assure une cardioprotection contre la toxicité des anthracyclines en inhibant la formation d'un complexe fer-anthracycline toxique.
Dexrazoxane : utilisation et disponibilité commerciale
Le dexrazoxane, un médicament cardioprotecteur approuvé par la FDA, a démontré son efficacité dans la gestion de la toxicité cardiaque associée à la chimiothérapie à base d'anthracycline chez les patients atteints de cancer, en particulier ceux atteints d'un cancer du sein avancé, de sarcomes des tissus mous ou d'un cancer du poumon à petites cellules. Il traite les lésions tissulaires causées par les anthracyclines. Le dexrazoxane est disponible sous des marques telles que Totect et Zinecard.
Structure et mécanisme d'action du dexrazoxane 
Le nom chimique du Dexrazoxane est 4,4′-[(1S)-1-Méthyl-1,2-éthanediyl]bis[2,6-pipérazinedione]. Sa formule chimique est C11H16N4O4, et son poids moléculaire est d'environ 268.27 g/mol.
Le dexrazoxane pénètre facilement dans les membranes cellulaires et est un dérivé cyclique de l'EDTA.
Impuretés et synthèse du dexrazoxane
Lors de la synthèse1 du Dexrazoxane, des impuretés sont générées comme sous-produits. Ils peuvent provenir de matières premières, de réactifs ou d’intermédiaires de réaction utilisés dans la fabrication. Il est nécessaire d'identifier et de caractériser ces impuretés pour garantir la pureté et la sécurité du produit final. Les techniques analytiques telles que la chromatographie liquide haute performance (HPLC) et la spectrométrie de masse (MS) contribuent au profilage et à la quantification des impuretés. Les fabricants de Dexrazoxane surveillent de près les impuretés pour répondre aux normes réglementaires et mettent en œuvre des méthodes de purification pour minimiser leur présence, garantissant ainsi la plus haute qualité du médicament à usage thérapeutique.
Daicel Pharma propose un certificat d'analyse (CoA) pour les étalons d'impuretés dexrazoxane, telles que l'impureté dexrazoxane-A, l'impureté dexrazoxane-C et l'impureté dexrazoxane-D, générés à partir d'une installation d'analyse conforme aux normes cGMP. Le CoA comprend un rapport de caractérisation complet comprenant des données provenant de techniques telles que la RMN 1H, la RMN 13C, l'IR, la MASS et la pureté HPLC.2. De plus, sur demande, nous fournissons des données supplémentaires telles que 13C-DEPT et CHN. Daicel Pharma peut synthétiser des impuretés ou des produits de dégradation inconnus du Dexrazoxane. Un rapport de caractérisation complet accompagne chaque livraison.
Bibliographie
FAQ
Bibliographie
- Creighton, Andrew M., dérivés de la 3,5-dioxopipérazine, National Research Development Corp., GB1374979A, 20 novembre 1974
- Rosing, H. ; van Gijn, R. ; dix Bokkel Huinink, WW ; Beijnen, JH, Analyse chromatographique liquide haute performance de l'agent cardioprotecteur dexrazoxane dans le plasma et l'urine humains, Journal of Liquid Chromatography & Related Technologies, Volume : 20, Numéro : 4, Pages : 583-601, 1997
Foire aux Questions
Quelles sont les impuretés courantes présentes dans le Dexrazoxane ?
Les impuretés courantes contenues dans le Dexrazoxane peuvent inclure des substances apparentées, des produits de dégradation, des solvants résiduels et d'autres contaminants liés au processus. Ils varient en fonction de la voie de synthèse et du procédé de fabrication.
Comment les impuretés du Dexrazoxane sont-elles éliminées lors de la purification du médicament ?
Les impuretés du Dexrazoxane sont éliminées lors des étapes de purification telles que la cristallisation, la filtration, la chromatographie et d'autres techniques de séparation. Ces méthodes permettent d'isoler le produit souhaité tout en éliminant les impuretés du mélange réactionnel.
Quel solvant aide à l’analyse des impuretés du Dexrazoxane ?
L'eau est un solvant utilisé pour analyser de nombreuses impuretés dans le Dexrazoxane.
Quelles sont les conditions de température nécessaires pour stocker les impuretés du Dexrazoxane ?
Les impuretés du dexrazoxane sont conservées à une température ambiante contrôlée entre 2 et 8 °C ou comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.