Charger plus
Vous avez vu 9 sur 32 articles
Daicel Pharma synthétise des impuretés du Darunavir d'une qualité exceptionnelle, telles que l'isomère (3R, 3aR, 6aS) -Darunavir, (3S, 3aR, 6aS) -isomère Darunavir, l'Amprenevir Oxazolone, le BIS THF HNS Derivative-I, et plus encore. Ces impuretés sont cruciales pour évaluer la pureté, la fiabilité et la sécurité d’un ingrédient pharmaceutique actif, le Darunavir. En outre, Daicel Pharma propose une synthèse personnalisée des impuretés du Darunavir pour répondre aux demandes de livraison des clients dans le monde entier.
Le darunavir [CAS : 206361/99/1] est un médicament antirétroviral essentiel classé comme inhibiteur de protéase, utilisé à la fois pour le traitement et la prévention de l'infection par le virus de l'immunodéficience humaine (VIH) et du syndrome d'immunodéficience acquise (SIDA). Il aide à gérer le VIH/SIDA en supprimant la réplication virale et en réduisant la progression de la maladie.
Le darunavir, disponible sous la marque Prezista, est un médicament antirétroviral destiné au traitement de l'infection par le virus de l'immunodéficience humaine (VIH-1). Il est administré en association avec d'autres médicaments antirétroviraux, soit du ritonavir à faible dose, soit du cobicistat, en fonction de l'âge et du poids du patient. Il s’agit d’un élément essentiel du traitement antirétroviral, en particulier pour les patients déjà sous TARV, contribuant à une prise en charge efficace du VIH et à l’amélioration des résultats pour les patients.
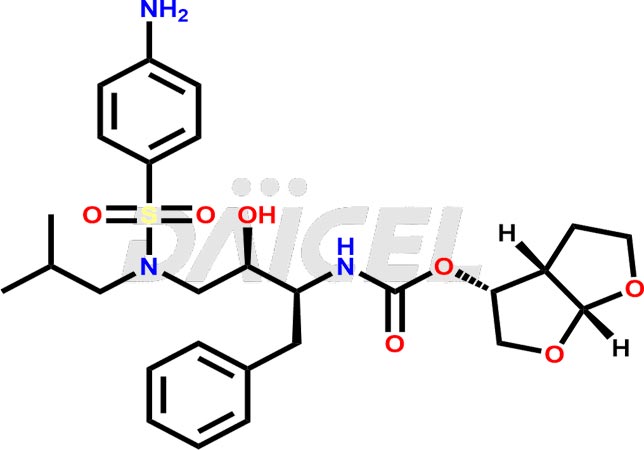
Le nom chimique du Darunavir est (3R,3aS,6aR)-Hexahydrofuro[2,3-b]furan-3-yl N-[(1S,2R)-3-[[(4-aminophényl)sulfonyl](2- méthylpropyl)amino]-2-hydroxy-1-(phénylméthyl)propyl]carbamate. Sa formule chimique est C27H37N3O7S, et son poids moléculaire est d'environ 547.7 g/mol.
Le darunavir bloque l'enzyme protéase qui reproduit le VIH. Le virus ne se reproduit pas normalement, ralentissant ainsi sa multiplication dans l’organisme.
Pendant la fabrication1, le stockage ou la dégradation du Darunavir, des impuretés se forment en raison de divers processus. Ces impuretés peuvent provenir des matières premières, des intermédiaires de réaction ou de la dégradation de la substance médicamenteuse. Des techniques analytiques telles que HPLC, LC et MS permettent d'analyser et de quantifier ces impuretés. Il est crucial de contrôler ces impuretés pour garantir la qualité, la sécurité et l'efficacité du Darunavir. Des mesures de contrôle strictes impliquent la définition de spécifications d’impuretés et la mise en œuvre de processus de fabrication robustes, ce qui est nécessaire.
Daicel Pharma propose un certificat d'analyse (CoA) pour les normes d'impuretés du Darunavir, telles que l'isomère (3R,3aR,6aS)-Darunavir, (3S,3aR,6aS)-isomère darunavir, l'Amprenevir Oxazolone, le BIS THF HNS Derivative-I et plus, généré à partir d’une installation d’analyse conforme aux normes cGMP. Le CoA comprend un rapport de caractérisation complet comprenant des données provenant de techniques telles que la RMN 1H, la RMN 13C, l'IR, la MASS et la pureté HPLC.2. De plus, sur demande, nous fournissons des données supplémentaires telles que 13C-DEPT et CHN. Daicel Pharma peut synthétiser des impuretés ou des produits de dégradation inconnus du Darunavir. Un rapport de caractérisation complet accompagne chaque livraison.
Oui, des études de stabilité sont menées pour surveiller les niveaux d'impuretés dans le Darunavir pendant sa durée de conservation, garantissant ainsi que les niveaux d'impuretés restent dans des limites acceptables.
Le contrôle des impuretés est un processus continu qui commence dès les premiers stades de développement et se poursuit tout au long du cycle de vie du Darunavir, y compris la surveillance après commercialisation.
L'acétonitrile est un solvant utilisé pour analyser de nombreuses impuretés du Darunavir.
Les impuretés du darunavir sont conservées à une température ambiante contrôlée entre 2 et 8 °C ou comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.