Daclatasvir
Renseignements généraux
Impuretés du Daclatasvir et Daclatasvir
Daicel Pharma synthétise l'impureté Daclatasvir d'une qualité exceptionnelle, le Daclatasvir Impureté G. Cette impureté est cruciale pour évaluer la pureté, la fiabilité et la sécurité d'un principe pharmaceutique actif, le Daclatasvir. En outre, Daicel Pharma propose une synthèse personnalisée des impuretés du Daclatasvir pour répondre aux demandes de livraison des clients dans le monde entier.
Daclatasvir [CAS : 1009119/64/5] est un médicament antiviral administré par voie orale qui cible spécifiquement la région de la protéine non structurale 5A (NS5A) du virus de l'hépatite C (VHC). Il traite les patients atteints d'hépatite C chronique.
Daclatasvir : utilisation et disponibilité commerciale
Le daclatasvir, disponible sous la marque Daklinza, en association avec le sofosbuvir, traite les infections chroniques par le virus de l'hépatite C (VHC) de génotype trois. Il cible la protéine NS5A du VHC et empêche la réplication virale.
Structure et mécanisme d'action du daclatasvir
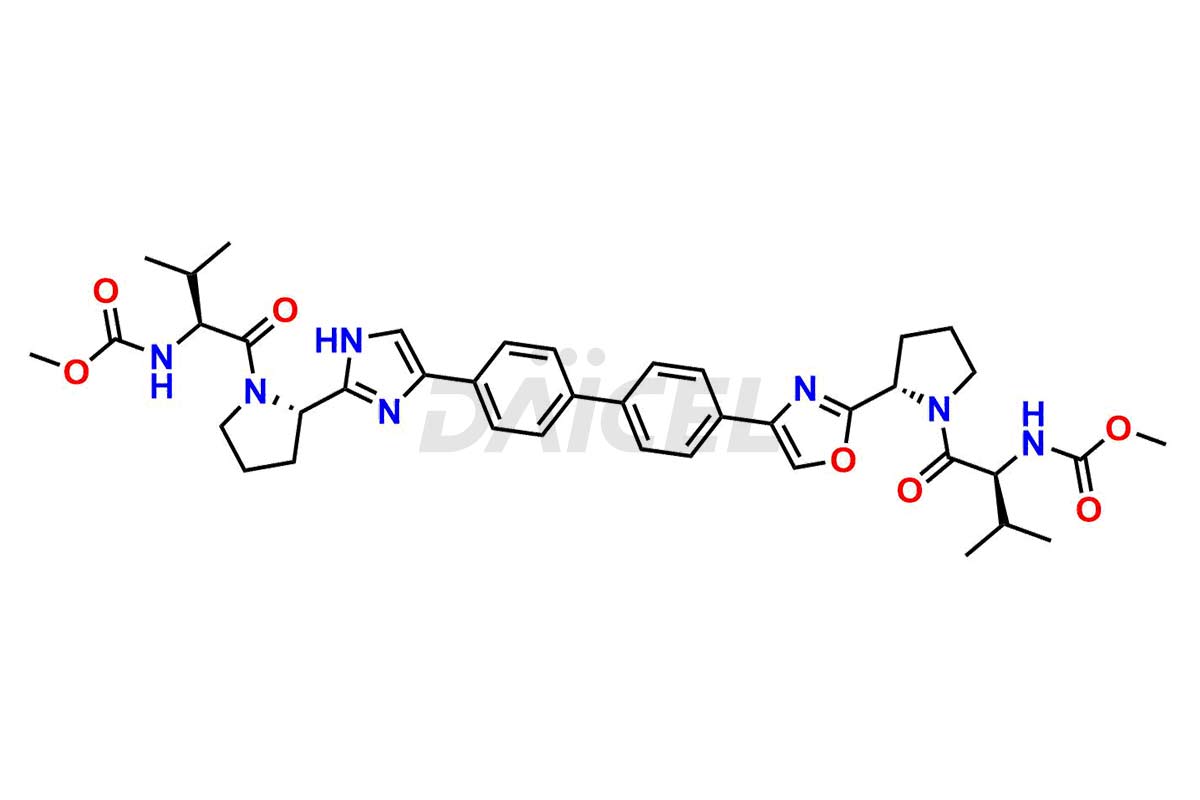
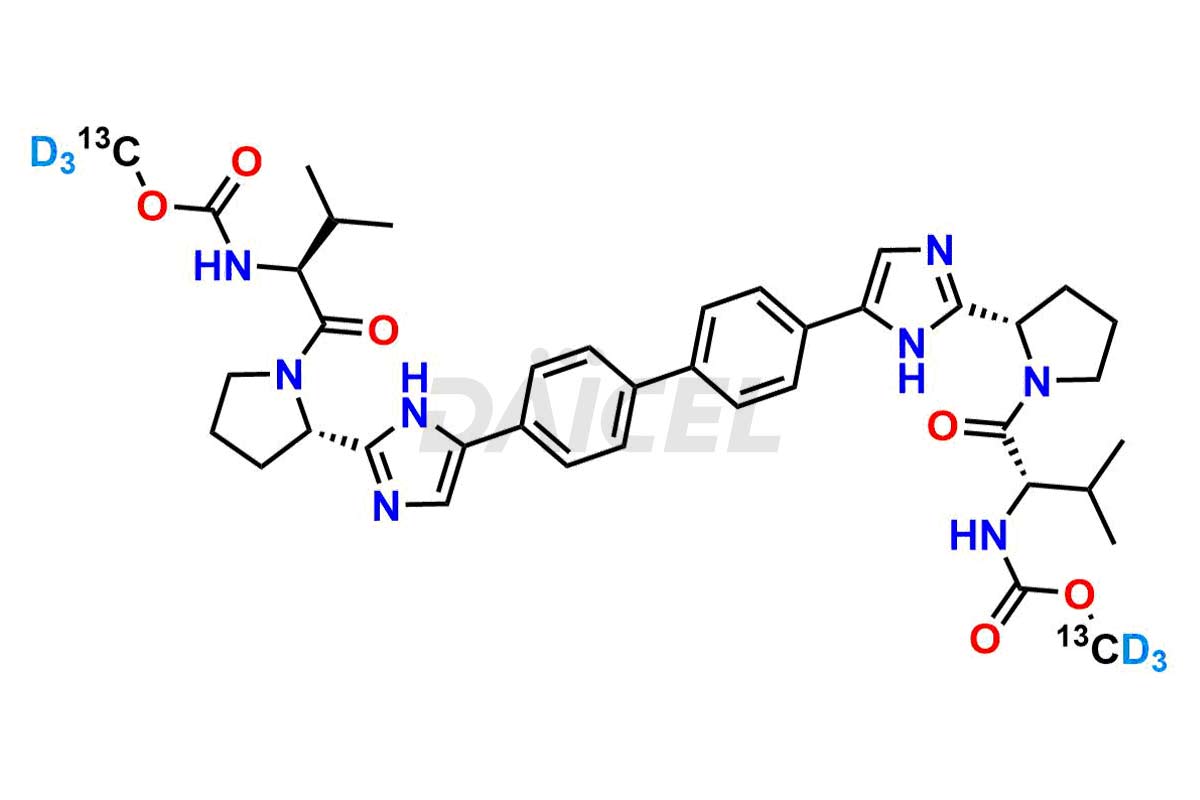
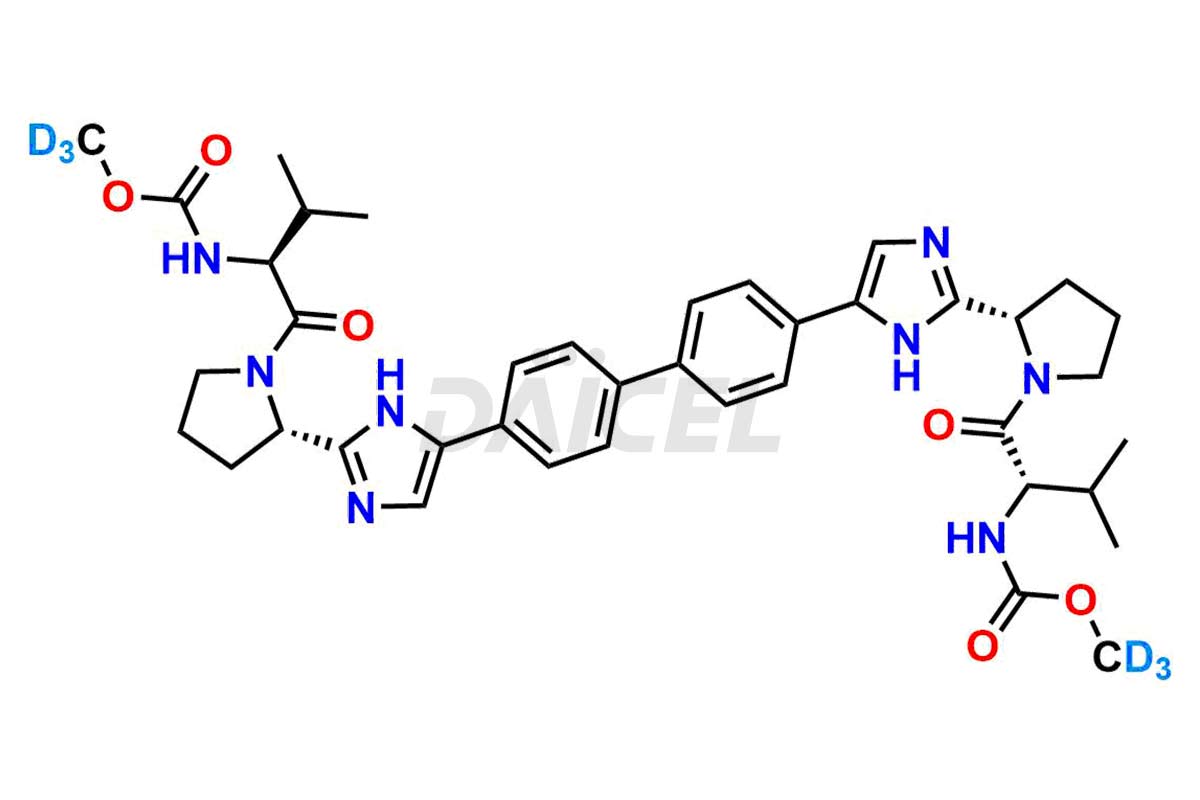
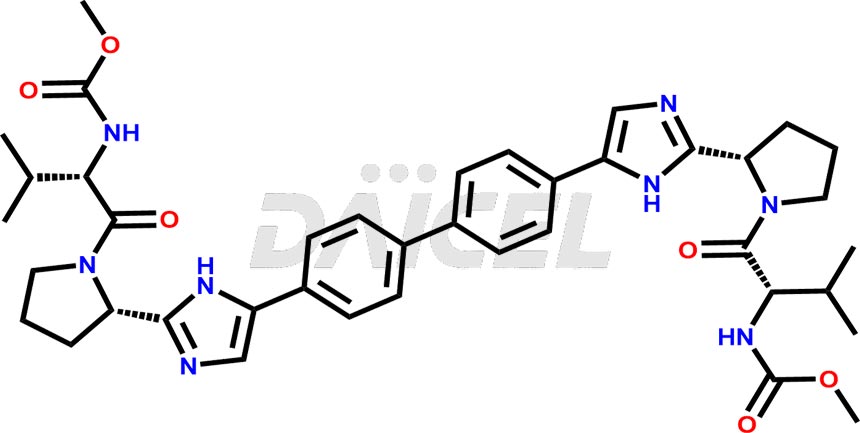
Le nom chimique du Daclatasvir est Acide carbamique, N, N′-[[1,1′-biphényl]-4,4′-diylbis[1H-imidazole-5,2-diyl-(2S)-2,1-pyrrolidinediyl. Ester de [(1S)-1-(1-méthyléthyl)-2-oxo-2,1-éthanediyl]]]bis-, C, C′-diméthyle. Sa formule chimique est C40H50N8O6, et son poids moléculaire est d'environ 738.9 g/mol.
Le daclatasvir inhibe la NS5A, une protéine non structurale codée par le virus de l'hépatite C. Il se lie à l’extrémité N-terminale de NS5A et empêche la réplication de l’ARN viral et l’assemblage des virions.
Impuretés et synthèse du Daclatasvir
Des impuretés de Daclatasvir se forment lors de la fabrication1, les processus de stockage ou de dégradation. Les techniques analytiques telles que HPLC, LC et MS aident à identifier et quantifier ces impuretés. Il est crucial de contrôler ces impuretés car elles peuvent affecter la qualité et la sécurité du Daclatasvir. Une mise en œuvre stricte de spécifications de contrôle des impuretés et de processus de fabrication robustes est nécessaire pour garantir la pureté et l’efficacité du médicament. Le respect des directives réglementaires et une surveillance continue sont essentiels pour maintenir la qualité et l'efficacité du Daclatasvir.
Daicel Pharma propose un certificat d'analyse (CoA) pour l'étalon d'impureté Daclatasvir, Daclatasvir Impurity G, généré à partir d'une installation d'analyse conforme aux normes cGMP. Le CoA comprend un rapport de caractérisation complet comprenant des données provenant de techniques telles que la RMN 1H, la RMN 13C, l'IR, la MASS et la pureté HPLC.2. De plus, sur demande, nous fournissons des données supplémentaires telles que 13C-DEPT et CHN. Daicel Pharma peut synthétiser des impuretés ou des produits de dégradation inconnus du Daclatasvir et des composés marqués pour évaluer l'efficacité du Daclatasvir générique. Nous proposons également le Daclatasvir-13C2D6 et le Daclatasvir-D6, des composés de Daclatasvir marqués au deutérium utiles dans la recherche bioanalytique, telle que les études BA/BE. Un rapport de caractérisation complet accompagne chaque livraison.
Bibliographie
FAQ
Bibliographie
- Bachand, Carol; Belema, Makonen; Déon, Daniel H. ; Bien, Andrew C. ; Goodrich, Jason ; James, Clint A. ; Lavoie, Rico; Lopez, Omar D. ; Martel, Alain; Meanwell, Nicolas A. ; et al, Inhibiteurs du virus de l'hépatite C, Bristol-Myers Squibb Company, États-Unis, US8329159B2, 11 décembre 2012
- Jiang, Hao ; Zeng, Jianing ; Kendoussi, Hamza ; Liu, Yifei ; Wang, Xiaodong ; Bifano, Marc; Cojocaru, Laura; Ryan, John ; Arnold, Mark E., Une méthode de spectrométrie de masse en tandem par chromatographie liquide sensible et précise pour la détermination quantitative du nouvel inhibiteur de l'hépatite C NS5A, BMS-790052 (daclastasvir) dans le plasma et l'urine humains, Journal of Chromatography A, Volume : 1245, Pages : 117-121, 2012
Foire aux Questions
Comment les matières premières sont-elles testées pour détecter les impuretés dans la production du Daclatasvir ?
Des procédures rigoureuses de contrôle de qualité, y compris les tests et la qualification des matières premières, sont mises en œuvre pour garantir leur pureté et leur adéquation à la fabrication du Daclatasvir.
Les impuretés du Daclatasvir peuvent-elles avoir un impact sur son efficacité thérapeutique ?
Certaines impuretés du Daclatasvir peuvent affecter son efficacité thérapeutique en interférant avec son mécanisme d'action ou en provoquant des effets indésirables dans l'organisme.
Quel solvant aide à l’analyse des impuretés du Daclatasvir ?
Le méthanol ou l'eau sont les solvants utilisés pour analyser de nombreuses impuretés du Daclatasvir.
Quelles sont les conditions de température nécessaires pour conserver les impuretés du Daclatasvir ?
Les impuretés du daclatasvir sont conservées à une température ambiante contrôlée entre 2 et 8 °C ou comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.