Charger plus
Vous avez vu 9 sur 14 articles
Daicel Pharma synthétise des impuretés de cyclophosphamide de haute qualité, du chlorhydrate de bis(3-chloroéthyl)phosphoramidate de 2-aminopropyle, des impuretés liées au cyclophosphamide (conduit d'éthanol à anneau fermé), des impuretés liées au cyclophosphamide (conduit d'éthanol à anneau ouvert) et du dihydroxybenzylcyclophosphamide, qui est crucial dans l'analyse de la qualité, la stabilité et la sécurité biologique du principe pharmaceutique actif, le cyclophosphamide. De plus, Daicel Pharma propose une synthèse personnalisée d'impuretés de cyclophosphamide et les livre dans le monde entier.
Cyclophosphamide [CAS : 50/18/0] est un médicament antinéoplasique apparenté aux moutardes azotées. Il s'agit d'un médicament alkylant destiné au traitement des maladies malignes et du syndrome néphrotique à changement minime chez les patients pédiatriques. Le cyclophosphamide est un puissant immunosuppresseur en réduisant les cellules T régulatrices à faibles doses.
Le cyclophosphamide est recommandé par la FDA américaine pour traiter les lymphomes malins, tels que le lymphome lymphocytaire, le lymphome de Burkitt, la maladie de Hodgkin, le lymphome lymphocytaire petit et le myélome multiple. Il est destiné au traitement du rétinoblastome, du cancer du sein, des adénocarcinomes ovariens, des neuroblastomes disséminés et du syndrome néphrotique à changement minime chez les patients pédiatriques. Le cyclophosphamide aide à traiter les maladies auto-immunes comme la sclérose en plaques en tant qu'agent immunosuppresseur puissant. Le cyclophosphamide est disponible sous des noms commerciaux tels que Cytoxan, Cytoxan lyophilisé et Neosar.
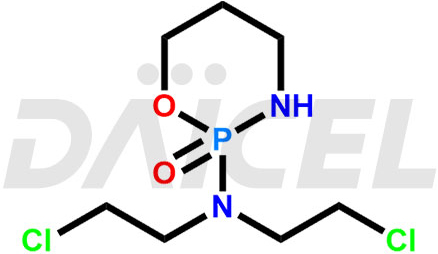
Le nom chimique du cyclophosphamide est 2-[Bis(2-chloroéthyl)amino]tétrahydro-2H-1,3,2-oxazaphosphorine 2-oxyde. Sa formule chimique est C7H15Cl2N2O2P, et son poids moléculaire est d'environ 261.09 g/mol.
Le cyclophosphamide implique la réticulation de l’ADN des cellules tumorales.
Le cyclophosphamide peut contenir diverses impuretés1 comme les composés apparentés, les produits de dégradation, etc., qui peuvent se former lors de la synthèse ou du stockage du médicament. Ces impuretés peuvent affecter la pureté, l’efficacité et la sécurité du médicament et doivent être surveillées pendant les processus de fabrication et de stockage.
Daicel propose un certificat d'analyse (CoA) d'un établissement d'analyse conforme aux BPF c pour les étalons d'impuretés du cyclophosphamide, le chlorhydrate de 3-aminopropylhydrogénosphosphamide (2-chloroéthyl)phosphoramidate, l'impureté liée au cyclophosphamide (aduct d'éthanol en anneau fermé), l'impureté associée au cyclophosphamide (anneau ouvert Ethanol Aduct) et dihydroxybenzylcyclophosphamide. Le CoA comprend des données de caractérisation complètes, telles que la RMN 1H, la RMN 13C2, IR, MASS et pureté HPLC. Nous fournissons également du 13C-DEPT et du CHN sur demande. Nous remettons un rapport de caractérisation complet à la livraison. Daicel possède la technologie et l'expertise nécessaires pour préparer toute impureté ou produit de dégradation inconnu du cyclophosphamide.
Le cyclophosphamide peut subir une dégradation et former des impuretés lorsqu'il est exposé à diverses conditions de stress, telles que l'hydrolyse acide ou basique, l'oxydation et la chaleur.
Le cyclophosphamide possède un spectre d'absorption UV caractéristique, ce qui permet de le détecter et de le quantifier à l'aide d'un détecteur UV. La concentration de Cyclophosphamide et de ses impuretés est déterminée en comparant l'absorption UV de l'échantillon à celle des standards connus.
Les impuretés peuvent affecter la qualité du cyclophosphamide en réduisant sa puissance, en modifiant sa pharmacocinétique ou sa pharmacodynamique, en provoquant des effets secondaires indésirables ou même en posant un risque pour la sécurité des patients.
Le contrôle des impuretés du cyclophosphamide est réglementé par divers organismes de réglementation internationaux tels que le Conseil international pour l'harmonisation des exigences techniques pour les produits pharmaceutiques à usage humain (ICH) et la Food and Drug Administration (FDA) des États-Unis.
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.