Cefprozil
Renseignements généraux
Impuretés du Cefprozil et Cefprozil
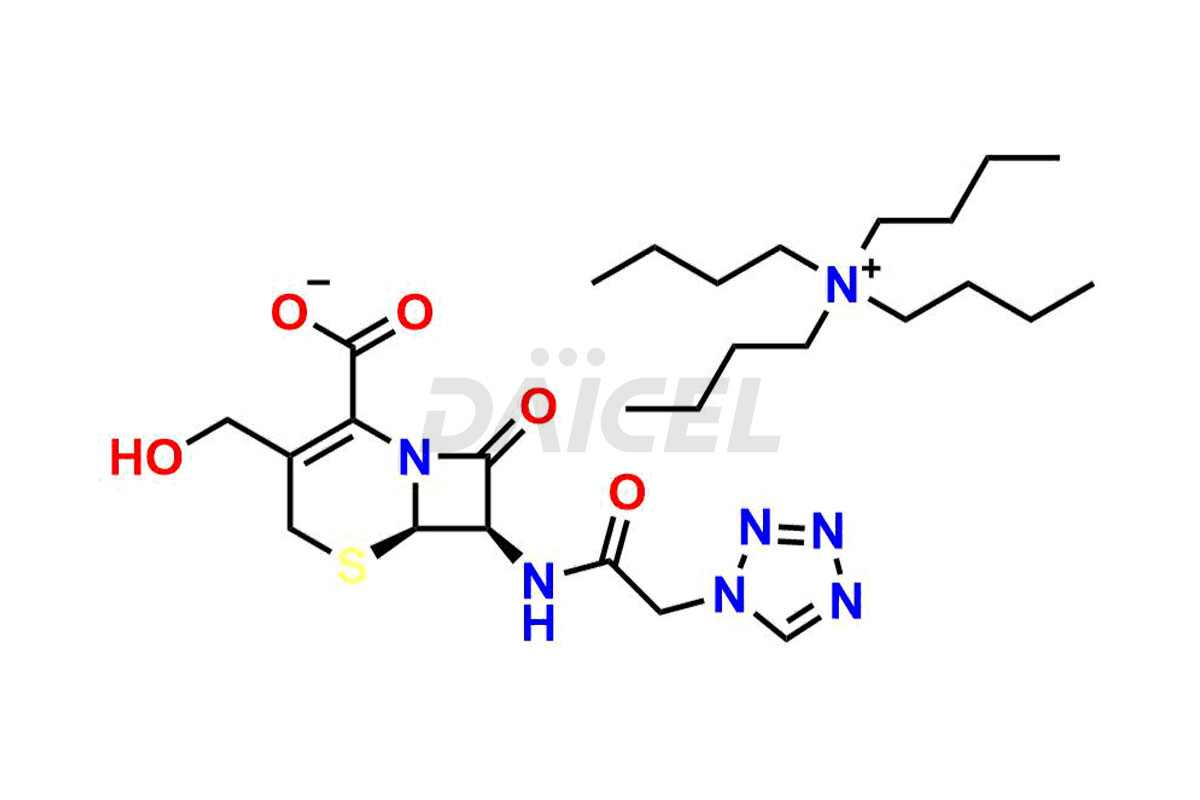
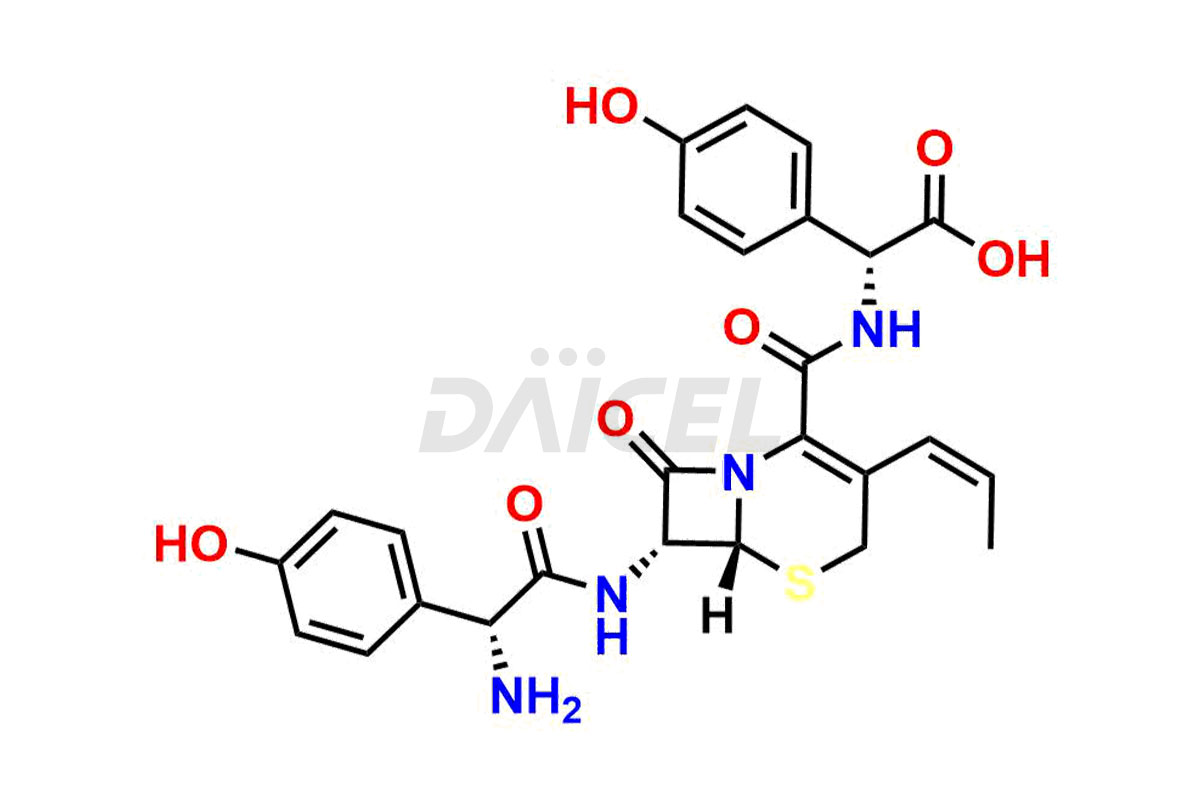
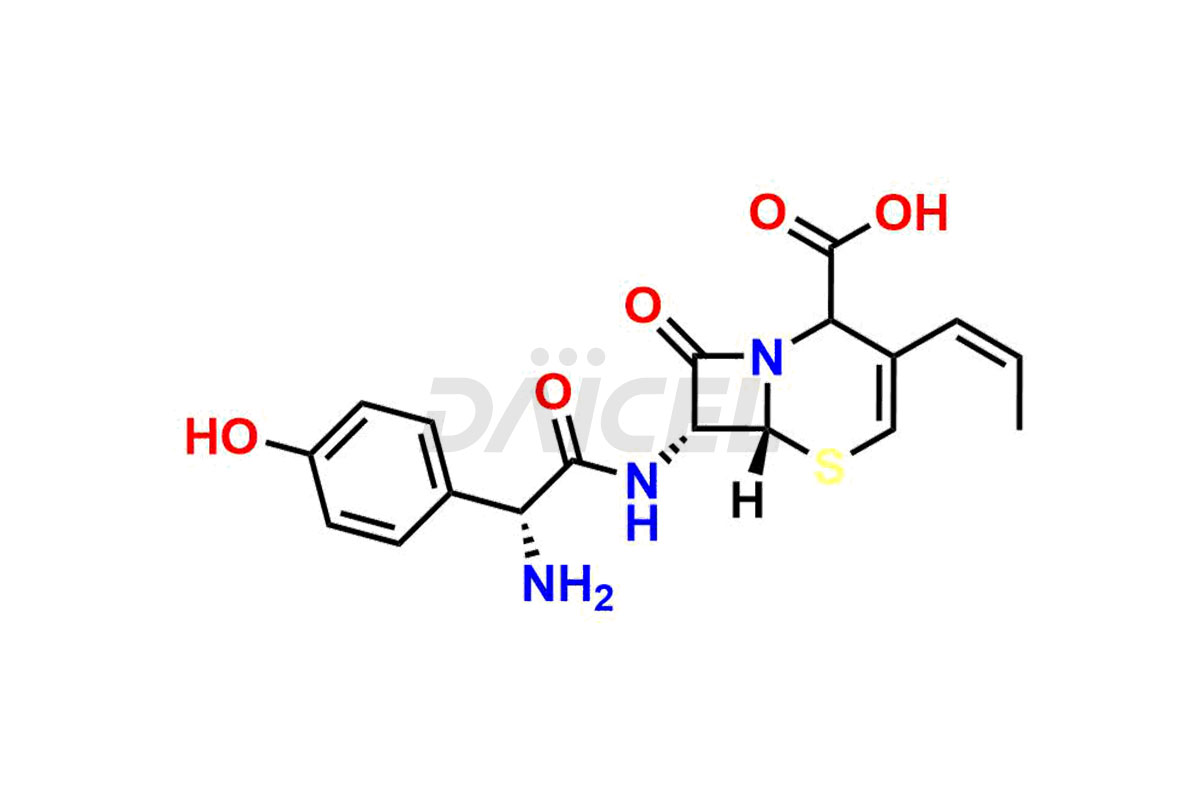
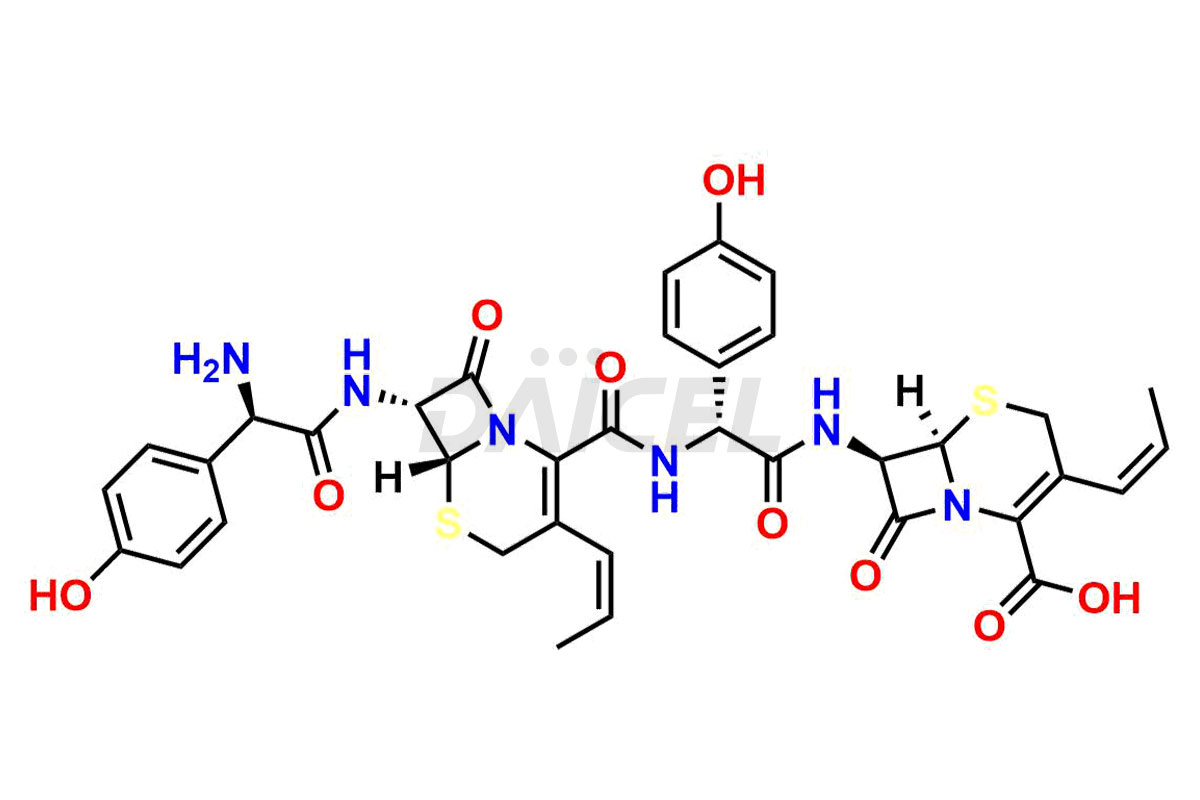
Daicel Pharma synthétise des impuretés de Cefprozil de qualité exceptionnelle, telles que l'impureté Cefazolin 3-hydroxy méthyle, l'amide de Cefprozil, l'isomère delta-3 de Cefprozil, le dimère de Cefprozil et l'impureté H de Cefprozil EP. Ces impuretés sont cruciales pour évaluer la pureté, la fiabilité et la sécurité du Cefprozil, un ingrédient pharmaceutique actif. En outre, Daicel Pharma propose une synthèse personnalisée des impuretés du Cefprozil pour répondre aux demandes de livraison des clients dans le monde entier.
Cefprozil [CAS : 92665/29/7] est un antibiotique bêta-lactamine de la classe des céphalosporines semi-synthétiques qui présente une activité bactéricide. Il traite la bronchite et les infections bactériennes affectant la peau, les oreilles et les systèmes respiratoires.
Cefprozil : utilisation et disponibilité commerciale
Le cefprozil est un antibiotique céphalosporine de deuxième génération dont la structure est similaire à celle du céfadroxil, une céphalosporine de première génération. Le cefprozil présente une activité contre diverses bactéries telles que S. pyogenes, S. pneumoniae, Neisseria spp., H. influenzae, M. catarrhalis, E. coli, P. mirabilis, Klebsiella et, dans une moindre mesure, les staphylocoques. Ses utilisations approuvées comprennent le traitement de l'otite moyenne aiguë, des infections bénignes des voies respiratoires inférieures, de la sinusite aiguë et des infections de la peau et des structures cutanées. Le Cefprozil traite les infections squelettiques suppurées chez les enfants. Il est disponible sous le nom commercial Cefzil.
Structure et mécanisme d'action du cefprozil 
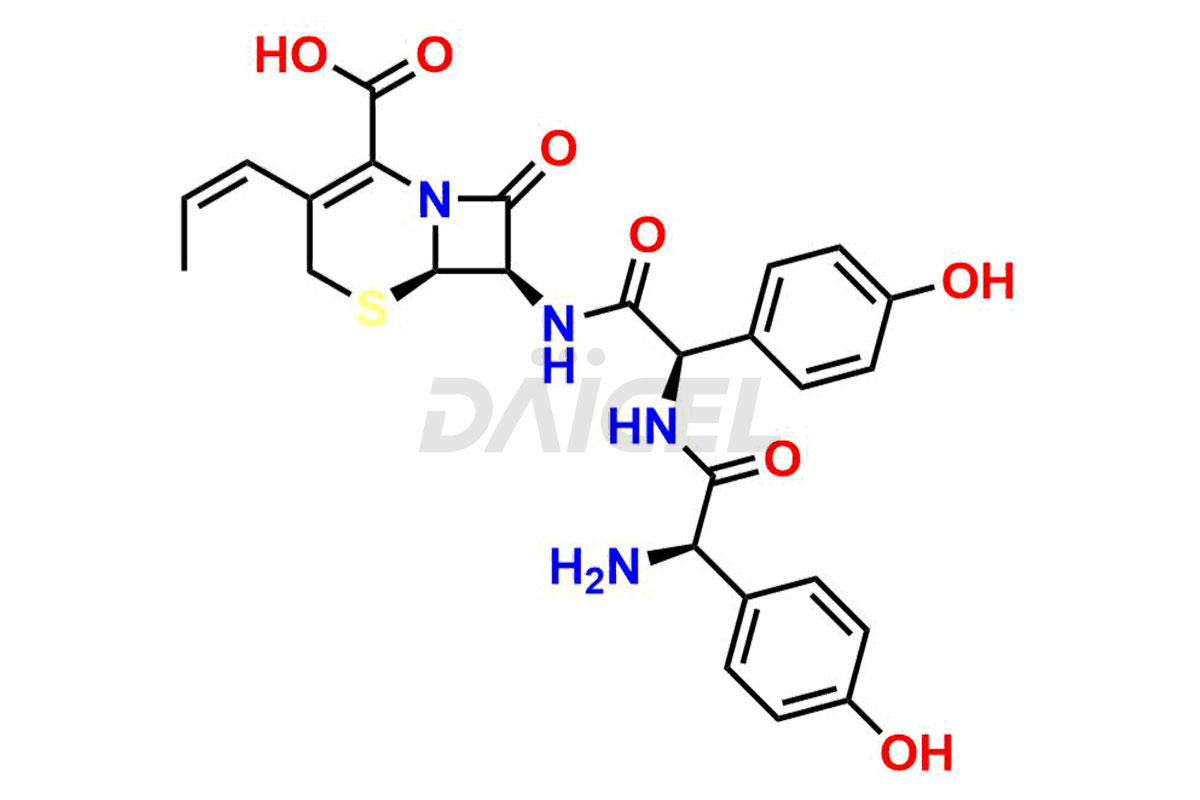
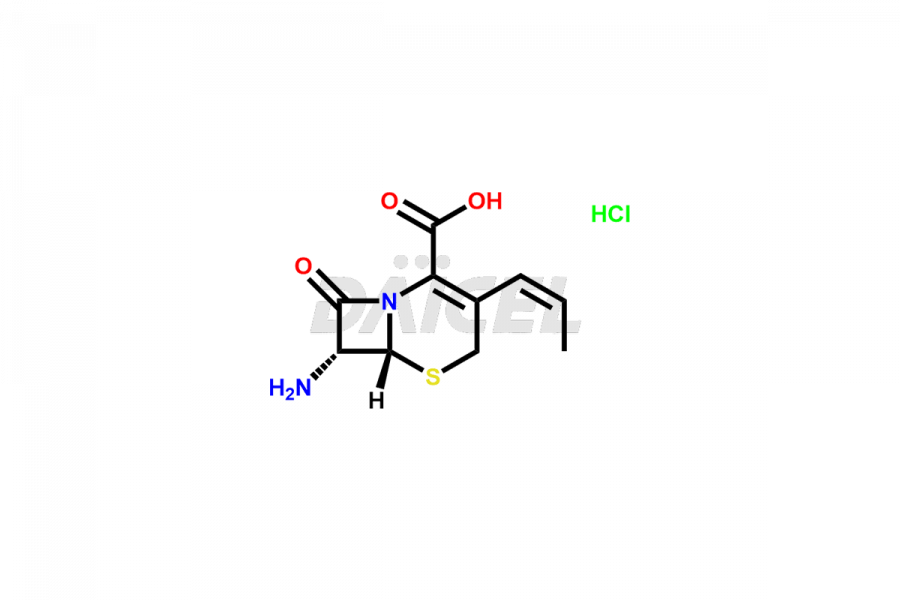
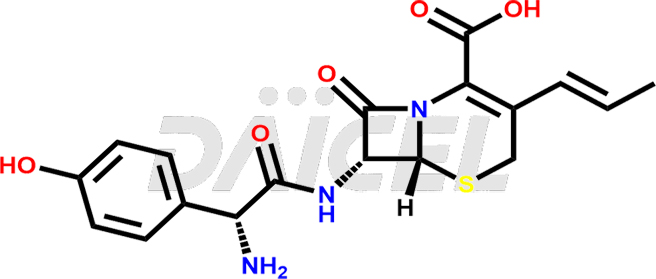
Le nom chimique du Cefprozil est (6R,7R)-7-[[(2R)-2-Amino-2-(4-hydroxyphényl)acétyl]amino]-8-oxo-3-(1-propén-1-yl). Acide )-5-thia-1-azabicyclo[4.2.0]oct-2-ène-2-carboxylique. Sa formule chimique est C18H19N3O5S, et son poids moléculaire est d'environ 389.4 g/mol.
Le cefprozil inhibe la synthèse de la paroi cellulaire bactérienne en se liant aux protéines liant la pénicilline (PBP) présentes dans la membrane cytoplasmique des bactéries.
Impuretés et synthèse du cefprozil
Des impuretés peuvent se former lors de la synthèse1 et stockage du Cefprozil, y compris les produits de dégradation2 et solvants résiduels. Ils affectent la qualité, la sécurité et l’efficacité du produit médicamenteux. Il est donc nécessaire de contrôler et de surveiller les niveaux d’impuretés du Cefprozil grâce à des méthodes analytiques appropriées lors de sa fabrication et de son stockage. Les autorités réglementaires ont établi des limites pour ces impuretés afin de garantir la qualité du produit médicamenteux.
Daicel Pharma propose un certificat d'analyse (CoA) pour les normes d'impuretés du Cefprozil, telles que l'impureté Cefazolin 3-hydroxy méthyle, l'amide de Cefprozil, l'isomère delta-3 du Cefprozil, le dimère du Cefprozil et l'impureté H du Cefprozil EP, générés à partir d'une installation d'analyse conforme aux normes cGMP. . Le CoA comprend un rapport de caractérisation complet comprenant des données provenant de techniques telles que la RMN 1H, la RMN 13C, l'IR, la MASS et la pureté HPLC. De plus, sur demande, nous fournissons des données supplémentaires telles que 13C-DEPT et CHN. Daicel Pharma peut synthétiser des impuretés ou des produits de dégradation inconnus du Cefprozil. Un rapport de caractérisation complet accompagne chaque livraison.
Bibliographie
FAQ
Bibliographie
- Hoshi, Hideaki ; Okumura, juin ; Abe, Yoshio ; Aburaki, Shimpei; Naito, Takayuki, Céphalosporines vinyliques substituées, Bristol-Myers Co., États-Unis, US4520022A, 28 mai 1985
- Daabees, HG; Mahrous, MS; Abdel-Khalek, MM; Beltagy, YA; Michail, Karim, Détermination spectrophotométrique du cefprozil dans les formes posologiques pharmaceutiques, dans l'urine et en présence de ses produits de dégradation induits alcalins, Analytical Letters, Volume : 34, Numéro : 10, Pages : 1639-1655, 2001
Foire aux Questions
Quelles sont les exigences réglementaires pour le contrôle des impuretés présentes dans le Cefprozil ?
Les autorités réglementaires exigent que les sociétés pharmaceutiques identifient et contrôlent les impuretés présentes dans Cefprozil conformément à des directives spécifiques et démontrent leur conformité à ces exigences.
Les impuretés contenues dans le Cefprozil peuvent-elles affecter sa biodisponibilité ?
Oui, les impuretés contenues dans Cefprozil peuvent affecter sa biodisponibilité et entraîner une diminution de l'absorption ou une modification de la pharmacocinétique.
Quelles mesures aident à empêcher la formation d'impuretés de Cefprozil dans le médicament pendant le stockage ?
Le Cefprozil est conservé dans des conditions spécifiques, notamment un contrôle de la température et de l'humidité, afin d'éviter la formation d'impuretés.
Quelles sont les conditions de température nécessaires pour conserver les impuretés de Cefprozil ?
Les impuretés de Cefprozil sont conservées à une température ambiante contrôlée entre 2 et 8 °C ou comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.