Charger plus
Vous avez vu 9 sur 11 articles
Daicel Pharma synthétise plus de dix impuretés de céfadroxil de haute qualité, telles que le dimère de céfadroxil, l'impureté H de céfadroxil, l'impureté A de céfadroxil EP, le composé D apparenté au céfadroxil, l'homologue d'éthyl céfadroxil, le méthoxy céfadroxil, le N-phénylglycyl céfadroxil, le dérivé de dicétopipérazine, le 7-éthoxycarbonyl 7- ADCA, et plus encore, qui aident à déterminer la qualité, la stabilité et la sécurité biologique de l'ingrédient pharmaceutique actif, le céfadroxil. De plus, Daicel Pharma propose une synthèse personnalisée des impuretés du céfadroxil et les livre dans le monde entier.
Cefadroxil [CAS : 50370-12-2] est un médicament antibactérien appartenant à la classe des céphalosporines.
Le céfadroxil est un antibiotique céphalosporine semi-synthétique de première génération. Il s’agit de traiter l’amygdalite, la pharyngite, les infections de la peau et des structures cutanées et les infections des voies urinaires. Il est efficace contre les infections causées par diverses souches bactériennes telles que Staphylococcus, les staphylocoques négatifs, H. influenzae, E. coli, S. pneumoniae, P. mirabilis, Streptococcus pyogenes (streptocoques bêta-hémolytiques du groupe A) et Klebsiella sp. Le médicament est disponible sous plusieurs noms commerciaux, dont Duricef et Ultracef.
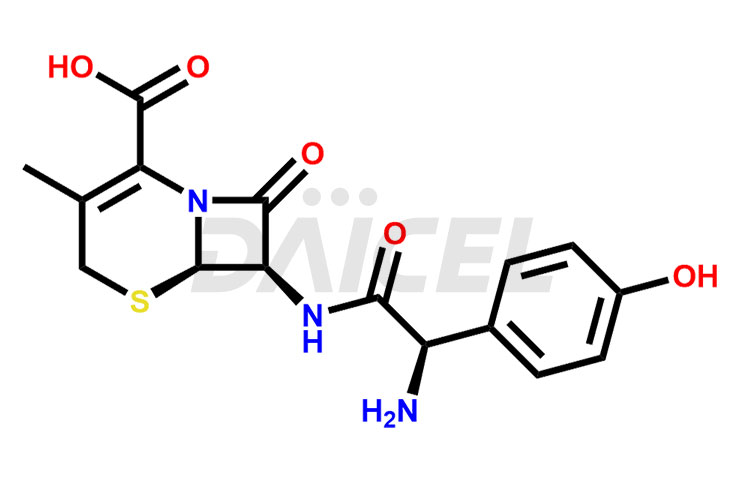
Le nom chimique du céfadroxil est (6R,7R)-7-[[(2R)-2-Amino-2-(4-hydroxyphényl)acétyl]amino]-3-méthyl-8-oxo-5-thia-1-. acide azabicyclo[4.2.0]oct-2-ène-2-carboxylique. Sa formule chimique est C16H17N3O5S, et son poids moléculaire est d'environ 363.4 g/mol.
Le céfadroxil se lie à certaines protéines liant la pénicilline (PBP) dans la paroi cellulaire bactérienne, comme d'autres antibiotiques bêta-lactamines. Cette action entrave la troisième et dernière phase de formation de la paroi cellulaire bactérienne. De plus, la désintégration cellulaire peut se produire par des enzymes autolytiques de la paroi bactérienne telles que les autolysines.
Certaines impuretés trouvées dans le céfadroxil comprennent des produits de dégradation, des solvants résiduels et des ions métalliques. Des produits de dégradation se forment en raison de l'exposition à la chaleur, à l'humidité et à des conditions acides ou alcalines. Les solvants résiduels qui existent après le processus de fabrication provoquent la formation d'impuretés. Les ions métalliques utilisés lors de la synthèse ou du stockage provoquent des impuretés. La présence de ces impuretés affecte la qualité, la sécurité et l’efficacité du médicament final. Il est donc essentiel de réduire les impuretés lors de la synthèse et purification1 de Cefadroxil et analyser et caractériser en profondeur le produit final pour garantir sa sécurité et son efficacité.
Daicel propose un certificat d'analyse (CoA) d'un centre d'analyse conforme aux BPF c pour plus de dix normes d'impuretés du céfadroxil, y compris le dimère de céfadroxil, l'impureté H du céfadroxil, l'impureté A du céfadroxil EP, le composé D apparenté au céfadroxil, l'homologue d'éthyle céfadroxil, le méthoxy céfadroxil, N-phénylglycyl céfadroxil, dérivé de dicétopipérazine, 7-éthoxycarbonyl 7-ADCA, et plus encore. Le CoA comprend des données de caractérisation complètes, telles que la RMN 1H, la RMN 13C, l'IR, la MASS et la HPLC. pureté2,3. Nous fournissons également du 13C-DEPT et du CHN sur demande. De plus, nous remettons un rapport de caractérisation complet à la livraison. Daicel possède la technologie et l'expertise nécessaires pour préparer toute impureté ou produit de dégradation inconnu du céfadroxil. La société fournit également des composés étiquetés pour quantifier l’efficacité du céfadroxil générique. Daicel propose des étalons de céfadroxil marqués par des isotopes hautement purs pour la recherche bioanalytique et les études BA/BE avec des données de pureté isotopique dans le CoA.
Les méthodes analytiques utilisées pour la détection des impuretés dans le céfadroxil comprennent la chromatographie liquide haute performance (HPLC), la spectrométrie de masse par chromatographie liquide (LC-MS), etc.
Les impuretés contenues dans le céfadroxil peuvent affecter sa sécurité en provoquant des effets indésirables chez les patients, tels que des réactions allergiques, une toxicité et des lésions organiques.
Les impuretés contenues dans le céfadroxil peuvent affecter la biodisponibilité du médicament en modifiant ses propriétés pharmacocinétiques, telles que l'absorption, la distribution, le métabolisme et l'excrétion.
L'élimination des impuretés du céfadroxil peut se faire par diverses techniques de purification, telles que la recristallisation, la chromatographie sur colonne et la HPLC préparative.
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.