Charger plus
Vous avez vu 9 sur 16 articles
Daicel Pharma synthétise des impuretés de cabozantinib de qualité exceptionnelle, telles que le monohydroxysulfate de cabozantinib, le N-oxyde de cabozantinib, le produit de clivage amide de cabozantinib, le dimère CBT, le CBT 2-fluoro, le CBT 3-fluoro, etc. Ces impuretés sont cruciales pour évaluer la pureté, la fiabilité et la sécurité du cabozantinib, un ingrédient pharmaceutique actif. En outre, Daicel Pharma propose une synthèse personnalisée des impuretés du cabozantinib pour répondre aux demandes de livraison des clients dans le monde entier.
Cabozantinib [CAS : 849217/68/1] est un inhibiteur du récepteur de la tyrosine kinase (RTK) à petite molécule qui peut combattre le cancer. Ce puissant agent antinéoplasique traite les formes avancées de cancer médullaire de la thyroïde et de carcinome rénal résistant aux autres traitements. Le cabozantinib est une option thérapeutique prometteuse pour les patients atteints d'un cancer métastatique.
Le cabozantinib traite les cancers avancés comme le cancer médullaire métastatique de la thyroïde et le carcinome rénal avancé chez les patients ayant déjà suivi un traitement antiangiogénique. De plus, son utilisation est approuvée chez les patients atteints d'un carcinome hépatocellulaire avancé traités par sorafénib. Le cabozantinib est disponible sous deux marques : Cabometyx et Cometriq.
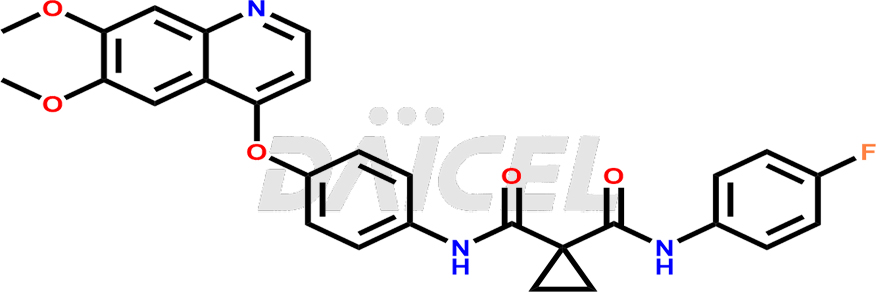
Le nom chimique du cabozantinib est N′-[4-[(6,7-Diméthoxy-4-quinolinyl)oxy]phényl]-N-(4-fluorophényl)-1,1-cyclopropane dicarboxamide. Sa formule chimique est C28H24FN3O5, et son poids moléculaire est d'environ 501.5 g/mol.
Le cabozantinib inhibe l'activité tyrosine kinase des récepteurs tyrosine kinases. Ils inhibent la croissance tumorale et conduisent à la régression tumorale.
Pendant la fabrication1 du cabozantinib, il se forme des impuretés qui peuvent être indésirables ou potentiellement nocives. Il doit être contrôlé pour garantir la sécurité et l’efficacité du produit final. Les impuretés du cabozantinib se forment par plusieurs réactions, comme l'oxydation, l'hydrolyse et la photolyse. Des méthodes telles que l'optimisation des processus, la purification et les tests analytiques aident à contrôler et à minimiser la formation d'impuretés dans le cabozantinib.
Daicel Pharma propose un certificat d'analyse (CoA) pour les étalons d'impuretés du cabozantinib, tels que le monohydroxysulfate de cabozantinib, le N-oxyde de cabozantinib, le produit de clivage amide de cabozantinib, le dimère CBT, le CBT 2-fluoro, le CBT 3-fluoro, etc., générés à partir de une installation d'analyse conforme aux normes cGMP. Le CoA comprend un rapport de caractérisation complet comprenant des données provenant de techniques telles que la RMN 1H, la RMN 13C, l'IR, la MASS et la pureté HPLC. De plus, sur demande, nous pouvons fournir des données supplémentaires telles que 13C-DEPT et CHN. Daicel Pharma peut synthétiser des impuretés ou des produits de dégradation inconnus du cabozantinib2. Un rapport de caractérisation complet accompagne chaque livraison.
Les impuretés du cabozantinib peuvent avoir des effets pharmacologiques inconnus et potentiellement nuire aux patients. Il est donc essentiel de les identifier et de les contrôler.
Les impuretés du cabozantinib ne peuvent pas être éliminées du produit médicamenteux, mais leurs niveaux peuvent être minimisés grâce à des processus de fabrication et à une surveillance efficaces.
Les impuretés du cabozantinib sont surveillées tout au long du processus de fabrication et pendant la durée de conservation du produit médicamenteux pour garantir que leurs niveaux restent dans des limites acceptables.
Les impuretés du cabozantinib sont conservées à une température ambiante contrôlée entre 2 et 8 °C ou comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.