Cabotégravir
Renseignements généraux
Impuretés du cabotégravir et cabotégravir
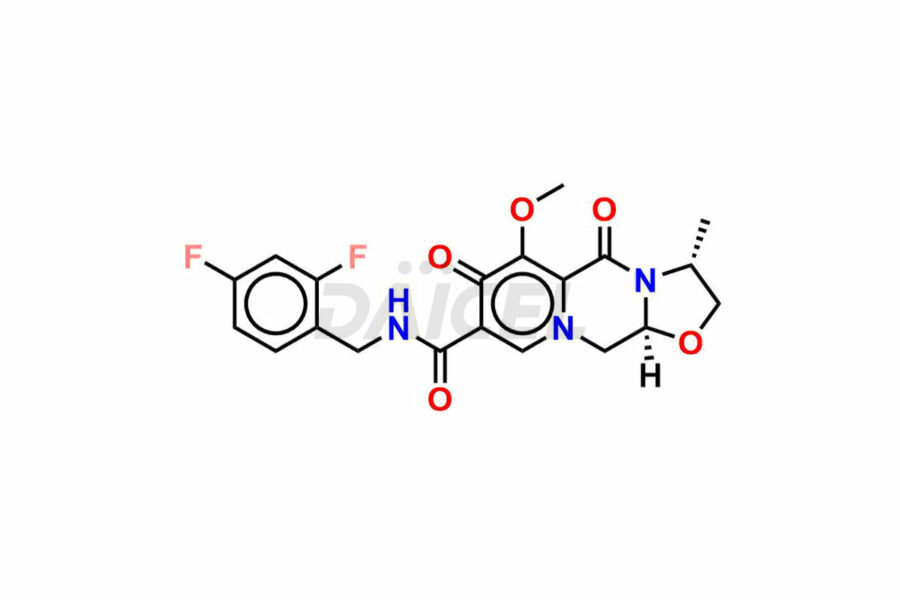
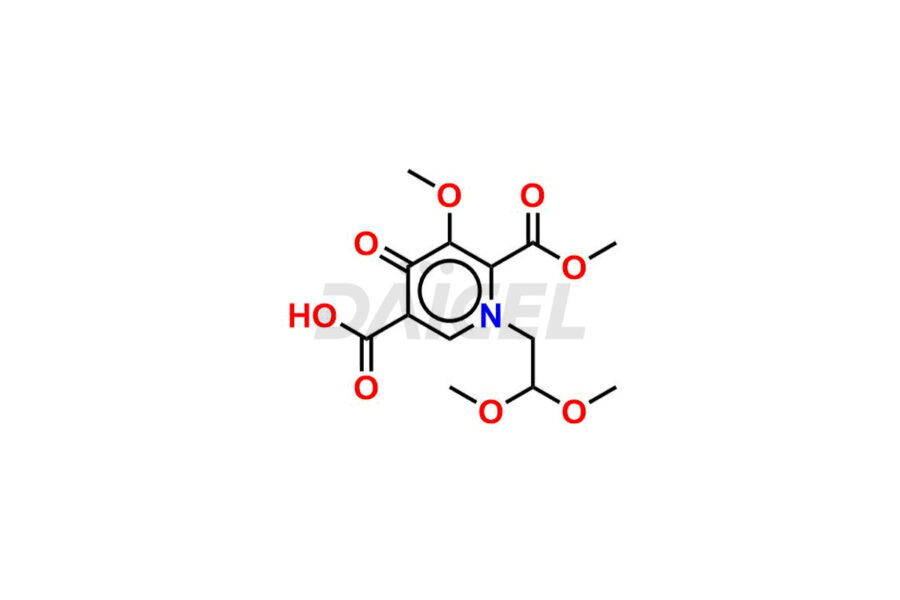
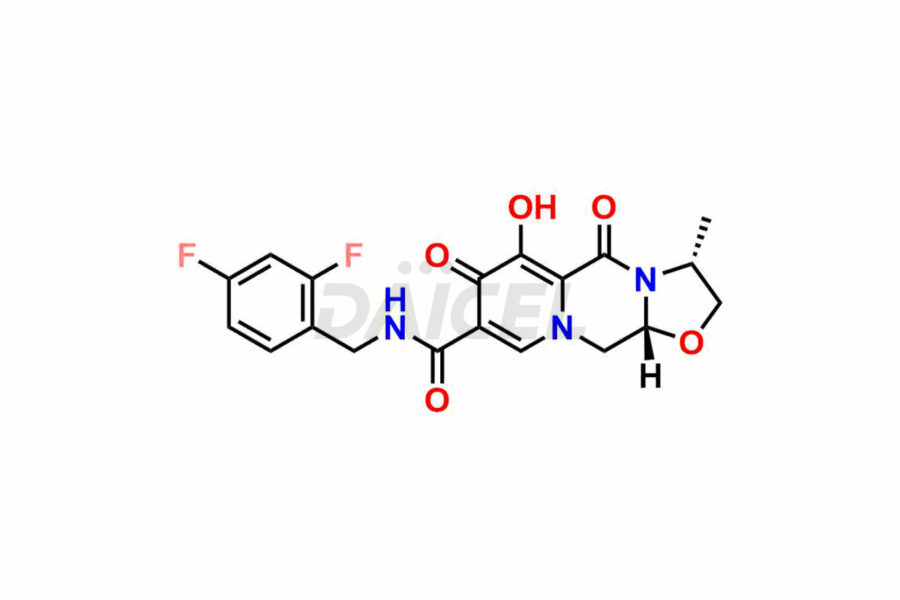
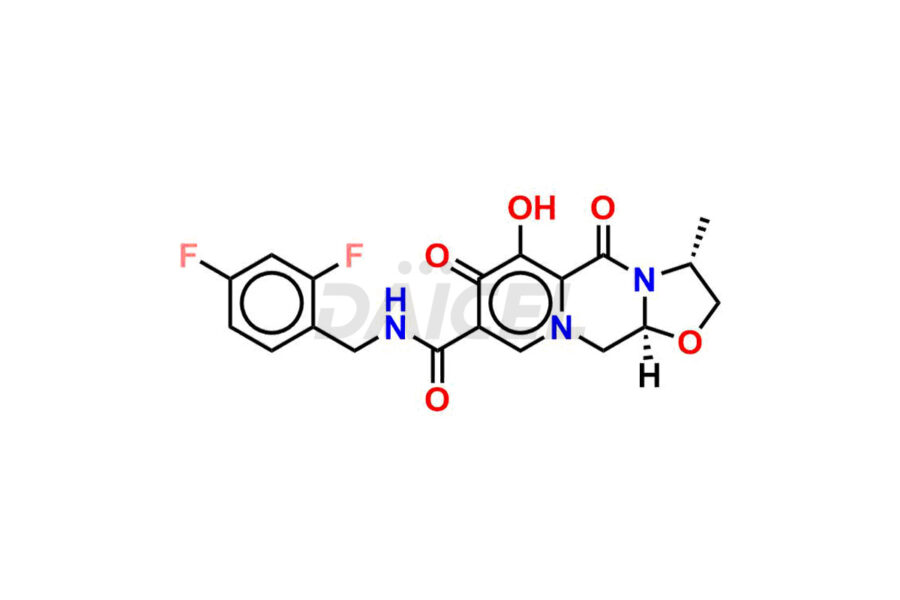
Daicel Pharma synthétise des impuretés du cabotégravir d'une qualité exceptionnelle, telles que l'impureté du cabotégravir 1, le cabotégravir intermédiaire-1, l'isomère du cabotégravir RR, l'isomère du cabotégravir RS et l'isomère du cabotégravir SS. Ces impuretés sont cruciales pour évaluer la pureté, la fiabilité et la sécurité du cabotegravir, un ingrédient pharmaceutique actif. En outre, Daicel Pharma propose une synthèse personnalisée des impuretés du cabotégravir pour répondre aux demandes de livraison mondiale de ses clients.
Cabotégravir [CAS : 1051375/10/0], également connu sous le nom de GSK1265744A, est un médicament destiné au traitement de l'infection par le VIH-1. Il s'agit d'un inhibiteur de l'intégrase, souvent prescrit en association avec la rilpivirine, un inhibiteur non nucléosidique de la transcriptase inverse. Le cabotégravir aide au traitement de l'infection par le VIH-1 chez les personnes présentant une suppression virale.
Cabotégravir : utilisation et disponibilité commerciale
Le cabotégravir est un médicament sur ordonnance sous deux formes et est disponible sous deux noms de marque. Vocabria est un comprimé oral en association avec un autre médicament anti-VIH appelé rilpivirine (Edurant) pour le traitement à court terme du VIH-1 chez les adultes, virologiquement supprimé. Apretude est une forme injectable à libération prolongée de cabotégravir qui traite les adultes et les adolescents à risque pesant au moins 35 kg pour une prophylaxie pré-exposition (PrEP) afin de réduire le risque d'infection par le VIH-1 sexuellement acquise.
Structure et mécanisme d'action du cabotégravir 
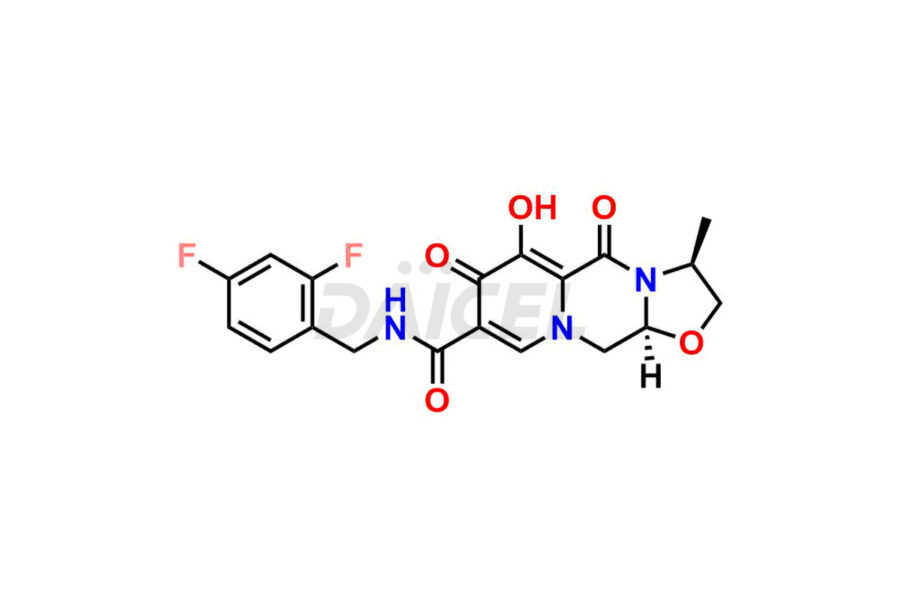
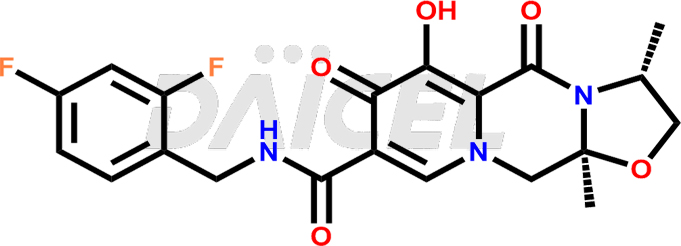
Le nom chimique du cabotegravir est (3S,11aR)-N-[(2,4-Difluorophényl)méthyl]-2,3,5,7,11,11a-hexahydro-6-hydroxy-3-méthyl-5,7. -dioxooxazolo[3,2-a]pyrido[1,2-d]pyrazine-8-carboxamide. Sa formule chimique est C19H17F2N3O5, et son poids moléculaire est d'environ 405.4 g/mol.
Le cabotégravir se lie au site actif de l'intégrase du VIH et inhibe l'intégrase du VIH. Il bloque l’étape de transfert de brin de l’intégration de l’acide désoxyribonucléique (ADN) rétroviral pour le cycle de réplication du VIH.
Impuretés et synthèse du cabotégravir
Comme toute autre substance pharmaceutique, le cabotegravir peut contenir des impuretés qui affectent sa sécurité et son efficacité. Ces impuretés se forment lors de la synthèse1, la purification et le stockage de la substance médicamenteuse. Ils peuvent inclure des impuretés liées au processus, telles que des matières premières, des réactifs, des intermédiaires et des produits de dégradation résultant de l'instabilité chimique ou physique de la substance médicamenteuse ou de sa formulation. La présence d'impuretés peut présenter des risques potentiels pour les patients, tels qu'une toxicité, une puissance réduite ou des effets indésirables. Il est donc essentiel de contrôler et de surveiller les niveaux d’impuretés du cabotegravir pour s’assurer qu’il répond aux normes de qualité et de sécurité requises pour les produits pharmaceutiques.
Daicel Pharma propose un certificat d'analyse (CoA) pour les normes d'impureté du cabotégravir, telles que l'impureté du cabotégravir 1, le cabotégravir intermédiaire-1, l'isomère du cabotégravir RR, l'isomère du cabotégravir RS et l'isomère du cabotégravir SS, générés à partir d'une installation d'analyse conforme aux normes cGMP. Le CoA comprend un rapport de caractérisation complet comprenant des données provenant de techniques telles que la RMN 1H, la RMN 13C, l'IR, la MASS et la pureté HPLC.2. De plus, sur demande, nous pouvons fournir des données supplémentaires telles que 13C-DEPT et CHN. Daicel Pharma peut synthétiser des impuretés ou des produits de dégradation inconnus du cabotegravir. Un rapport de caractérisation complet accompagne chaque livraison.
Bibliographie
FAQ
Bibliographie
- Johns, Brian Alvin ; Kawasuji, Takashi ; Taishi, Teruhiko ; Taoda, Yoshiyuki, Dérivé bicyclique de carbamoylpyridone ayant une activité inhibitrice de l'intégrase du VIH, Shionogi & Co., Ltd., Japon, EP1852434B1, 13 juillet 2011
- Krishna Murthy Kasa, SR; Venkatanarayana, Muvvala ; Chennuru, Lakshmi Narayana ; Chandra Sekhara Rao, B. ; Vemparala, Manohar ; Chaman, Abdul Fareed ; Talluri, MVN Kumar, Développement de la méthode Chiral LC : séparation stéréo-sélective, caractérisation et détermination du cabotégravir et des impuretés isomères RS, RR et SS associées sur une phase stationnaire chirale à base de cellulose enrobée par HILIC-LC et LC-MS, Journal of Analyse pharmaceutique et biomédicale, Volume : 222, Pages : 115062, 2023
Foire aux Questions
Comment les impuretés du cabotegravir sont-elles détectées et analysées ?
Les impuretés du cabotegravir sont détectées et analysées à l'aide de techniques analytiques telles que la chromatographie liquide haute performance (HPLC) et la chromatographie liquide-spectrométrie de masse (LC-MS). Ces techniques aident à l'identification et à la quantification des impuretés.
Comment les impuretés du cabotégravir peuvent-elles affecter la stabilité du produit médicamenteux ?
Les impuretés du cabotégravir peuvent affecter la stabilité du produit médicamenteux, avec un impact sur la puissance et l'efficacité du médicament. Le contrôle des impuretés est essentiel pour assurer la stabilité et la durée de conservation du produit médicamenteux.
Quel solvant aide à l’analyse des impuretés du Cabotégravir ?
L'acétonitrile ou le méthanol sont les solvants utilisés pour analyser de nombreuses impuretés du cabotegravir.
Quelles sont les conditions de température nécessaires pour stocker les impuretés du Cabotegravir ?
Les impuretés du cabotégravir sont conservées à une température ambiante contrôlée entre 2 et 8 °C ou comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.