Charger plus
Vous avez vu 9 sur 18 articles
Daicel Pharma synthétise des impuretés Brivaracétam de qualité exceptionnelle, telles que le Brivaracétam (alfa R, 4R)-Isomer (DS-2), le Brivaracétam (Alfa R, 4S)-Isomer (Enantiomer), le Brivaracétam (alfa S, 4S)-Isomer (DS- 1), Brivaracétam EP Impureté-D, Brivaracetam methyl ester (2S,4R) Isomer, et ainsi de suite. Ces impuretés sont cruciales pour évaluer la pureté, la fiabilité et la sécurité du Brivaracétam, un ingrédient pharmaceutique actif. En outre, Daicel Pharma propose une synthèse personnalisée des impuretés du Brivaracétam pour répondre aux demandes de livraison des clients dans le monde entier.
Brivaracétam [CAS : 357336/20/0] est un médicament anticonvulsivant utilisé en association avec d'autres médicaments pour traiter les crises partielles. Ce médicament disponible par voie orale est un dérivé du lévétiracétam.
Le brivaracétam est un anticonvulsivant de structure similaire au lévétiracétam. Il traite les épilepsies liées à la localisation et un spectre plus large de troubles épileptiques. Le nom commercial du Brivaracétam est Briviact.
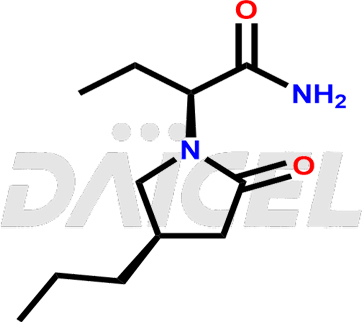
Le nom chimique du Brivaracétam est (αS,4R)-α-Ethyl-2-oxo-4-propyl-1-pyrrolidineacetamide. Sa formule chimique est C11H20N2O2, et son poids moléculaire est d'environ 212.29 g/mol.
Le brivaracétam a une affinité pour la protéine 2A des vésicules synaptiques (SV2A) du cerveau, conduisant à un effet anticonvulsivant. Mais son mécanisme d’action n’est pas connu.
Les impuretés contenues dans le Brivaracétam sont des impuretés organiques, des impuretés inorganiques et des solvants résiduels. Les impuretés organiques peuvent inclure des substances apparentées formées au cours du processus de synthèse1, les produits de dégradation dus à la chaleur, à la lumière ou à l'humidité, ainsi que les impuretés provenant des matières premières. Les impuretés inorganiques sont des métaux ou d'autres substances inorganiques pouvant apparaître lors de la fabrication. Des solvants résiduels peuvent également être présents dans le processus de fabrication. Ils doivent être surveillés et contrôlés dans des limites acceptables et selon les directives réglementaires pendant le développement du médicament.
Daicel Pharma propose un certificat d'analyse (CoA) pour les étalons d'impuretés du brivaracétam, tels que le brivaracétam (alfa R, 4R)-isomère (DS-2), le brivaracétam (Alfa R, 4S)-isomère (énantiomère), le brivaracétam (alfa S). , 4S) -Isomer (DS-1), Brivaracetam EP Impurity-D, Brivaracetam methyl ester (2S,4R) Isomer, etc., générés à partir d'une installation d'analyse conforme aux normes cGMP. Le CoA comprend un rapport de caractérisation complet comprenant des données provenant de techniques telles que la RMN 1H, la RMN 13C, l'IR, la MASS et la pureté HPLC.2. De plus, sur demande, nous pouvons fournir des données supplémentaires telles que 13C-DEPT et CHN. Daicel Pharma peut préparer des impuretés ou des produits de dégradation inconnus du Brivaracétam. Un rapport de caractérisation complet accompagne chaque livraison.
Les limites d'impuretés pour le Brivaracétam sont déterminées en fonction de l'innocuité et de l'efficacité. Les autorités de réglementation, telles que l'USP et l'ICH, régissent les limites d'impuretés.
Lors de la fabrication, des tests analytiques détectent et quantifient les impuretés potentielles dans la substance médicamenteuse Brivaracétam. Ces tests incluent HPLC, LC-GC, RMN et d’autres méthodes pour garantir la pureté de la substance médicamenteuse.
L'acétonitrile ou le méthanol sont des solvants utilisés pour analyser de nombreuses impuretés dans le brivaracétam.
Les impuretés du brivaracétam sont conservées à une température ambiante contrôlée entre 2 et 8 °C ou comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.