Charger plus
Vous avez vu 9 sur 11 articles
Daicel Pharma synthétise des impuretés Brinzolamide d'une qualité exceptionnelle, comme le Méthyl(S)-N-((4-hydroxy-2-(3-methoxypropyl)-1,1-dioxido-3,4-dihydro-2H-thieno[3,2 -e][1,2]thiazin-6-yl)sulfonyl)acétimidate de méthyle (S)-N-((2-(3-méthoxypropyl)-1,1-dioxido-4-(tosyloxy)-3,4 -dihydro-2H-thiéno[3,2-e][1,2]thiazin-6-yl)sulfonyl)acétimidate, (4R)-4-Hydroxy-2-(3-méthoxypropyl)-3,4-dihydro- 2H-thiéno[3,2-e][1,2] thiazine-6-sulfonamide 1,1 dioxyde, (4S)-6-chloro-2-(3-méthoxypropyl)-3,4-dihydro-2H-thiéno Dioxyde de [3,2-e] [1,2] thiazine-4-ol-1,1, et ainsi de suite. Ces impuretés sont cruciales pour évaluer la pureté, la fiabilité et la sécurité d’un ingrédient pharmaceutique actif, le brinzolamide. En outre, Daicel Pharma propose une synthèse personnalisée d'impuretés brinzolamide pour répondre aux demandes de livraison des clients dans le monde entier.
Brinzolamide [CAS : 138890/62/7] est un dérivé du sulfamide, agit comme un inhibiteur de l'enzyme anhydrase carbonique. C'est un médicament antiglaucomateux. Le brinzolamide réduit la pression intraoculaire élevée causée par le glaucome à angle ouvert, qui peut entraîner des lésions du nerf optique et une perte de vision s'il n'est pas traité.
Le brinzolamide abaisse la pression intraoculaire (PIO) chez les patients. Il inhibe l'anhydrase carbonique II (CA-II), supprime la formation d'humeur aqueuse et réduit la PIO. Le brinzolamide est un inhibiteur réversible de CA-II. Le brinzolamide est disponible sous le nom commercial Azopt.
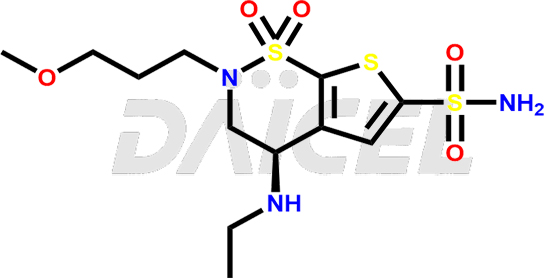
Le nom chimique du brinzolamide est (4R)-2H-Thieno[3,2-e]-1,2-thiazine-6-sulfonamide, 4-(éthylamino)-3,4-dihydro-2-(3-méthoxypropyle). - 1,1-dioxyde. Sa formule chimique est C12H21N3O5S3, et son poids moléculaire est d'environ 383.5 g/mol.
Le brinzolamide diminue la sécrétion d'humeur aqueuse, éventuellement en ralentissant la formation d'ions bicarbonate et en réduisant la pression intraoculaire. Cette réduction est bénéfique dans le traitement d’affections telles que le glaucome à angle ouvert.
Le brinzolamide peut contenir des impuretés, telles que des composés apparentés et des solvants résiduels, formés au cours du processus de fabrication.1 ou du stockage. Ils peuvent avoir un impact sur la sécurité et l’efficacité du produit médicamenteux. Certaines impuretés courantes du brinzolamide comprennent les produits de dégradation, les isomères et les solvants résiduels. Il est essentiel de contrôler et de surveiller ces impuretés par diverses méthodes, telles que le développement de processus de fabrication appropriés, l'utilisation de matières premières de haute qualité, la mise en œuvre de conditions de stockage appropriées et la réalisation de tests analytiques réguliers pendant la fabrication et tout au long de sa durée de conservation pour garantir la qualité du produit. produit médicamenteux. Ces mesures contribuent à garantir que le produit médicamenteux est sûr et efficace pour les patients.
Daicel Pharma propose un certificat d'analyse (CoA) pour les étalons d'impuretés brinzolamide, tels que le méthyle (S)-N-((4-hydroxy-2-(3-méthoxypropyl)-1,1-dioxido-3,4-dihydro- 2H-thiéno[3,2-e][1,2]thiazin-6-yl)sulfonyl)acétimidate de méthyle (S)-N-((2-(3-méthoxypropyl)-1,1-dioxido-4- (tosyloxy)-3,4-dihydro-2H-thiéno[3,2-e][1,2]thiazin-6-yl)sulfonyl)acétimidate, (4R)-4-Hydroxy-2-(3-méthoxypropyle) -3,4-dihydro-2H-thiéno[3,2-e][1,2] thiazine-6-sulfonamide 1,1 dioxyde, (4S)-6-chloro-2-(3-méthoxypropyl)-3,4, Le dioxyde de 2-dihydro-3,2H-thiéno[1,2-e] [4] thiazine-1,1-ol-1, etc., généré à partir d'une installation d'analyse conforme aux normes cGMP. Le CoA comprend un rapport de caractérisation complet comprenant des données provenant de techniques telles que la RMN 13H, la RMN XNUMXC, l'IR, la MASS et la pureté HPLC.2. De plus, sur demande, nous pouvons fournir des données supplémentaires telles que 13C-DEPT et CHN. Daicel Pharma peut préparer des impuretés ou des produits de dégradation inconnus du brinzolamide. Un rapport de caractérisation complet accompagne chaque livraison.
Diverses méthodes sont utilisées pour contrôler les impuretés du brinzolamide, telles que le contrôle du processus de fabrication, l'utilisation de conditions d'emballage et de stockage appropriées et l'utilisation de méthodes analytiques pour détecter et quantifier les impuretés.
Oui, les impuretés contenues dans le brinzolamide peuvent affecter son efficacité thérapeutique et modifier l'activité pharmacologique et la biodisponibilité du médicament, entraînant des effets indésirables ou une efficacité réduite.
L'acétonitrile est un solvant utilisé dans l'analyse de nombreuses impuretés du brinzolamide.
Les impuretés du brinzolamide sont conservées à une température ambiante contrôlée entre 2 et 8 °C ou -20 °C, selon la stabilité de l'impureté, comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.