Bosutinib
Renseignements généraux
Impuretés du bosutinib et bosutinib
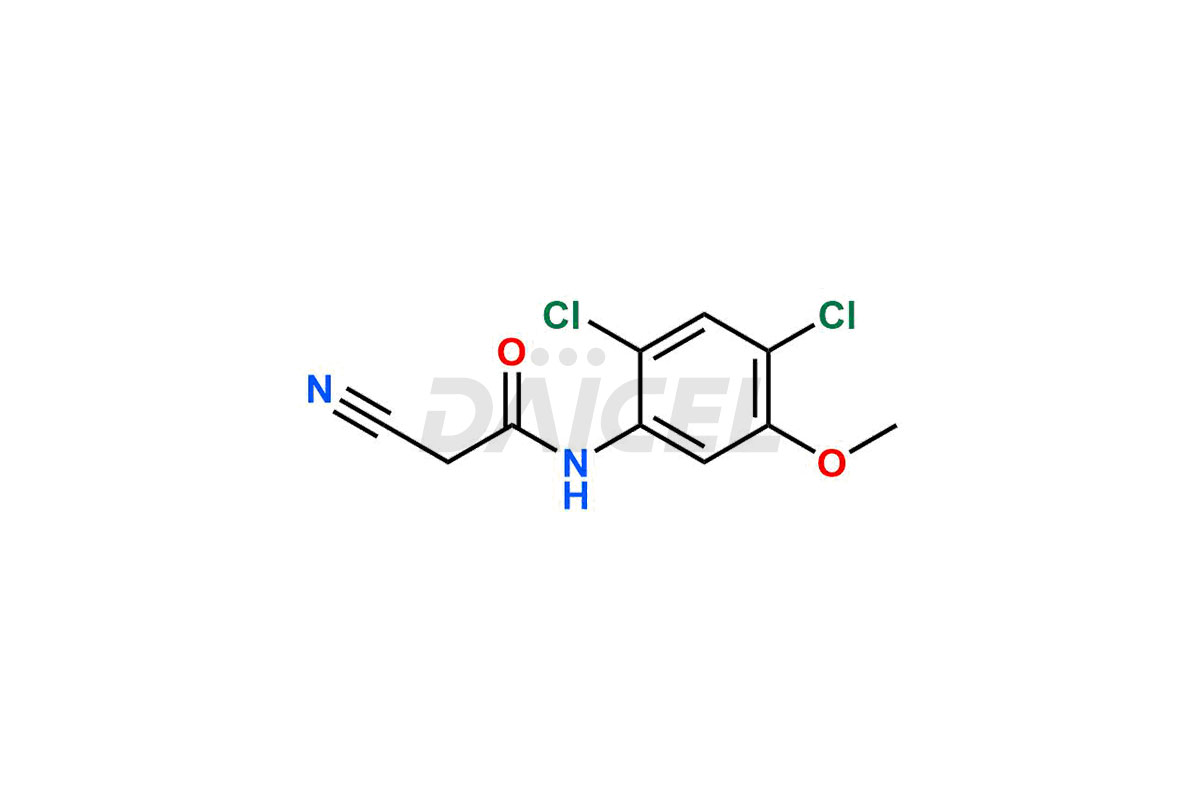
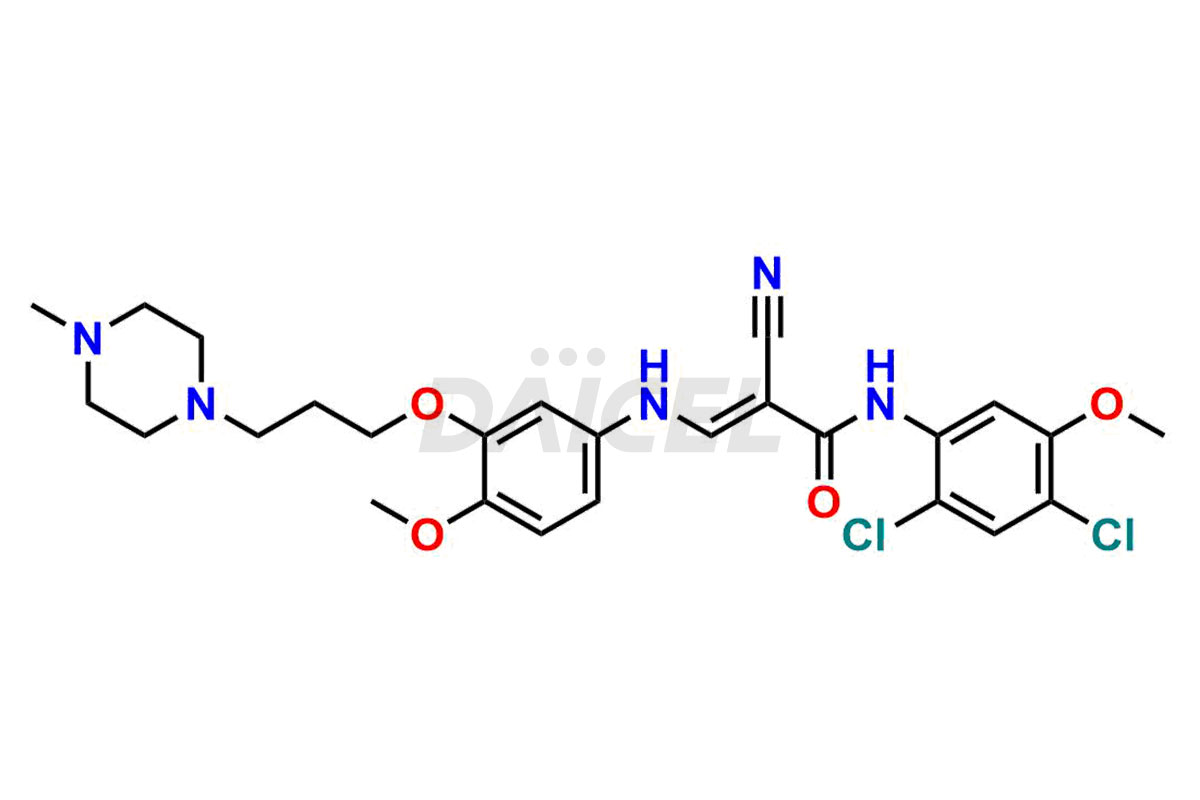
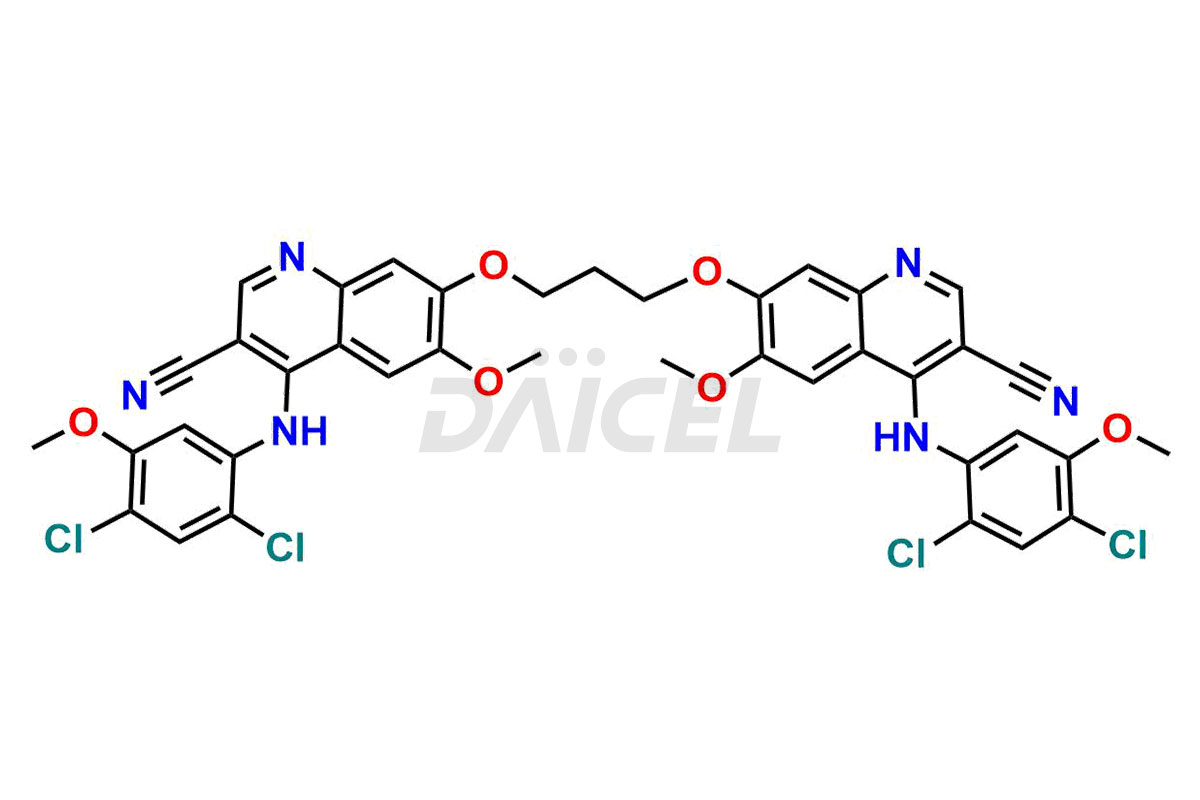
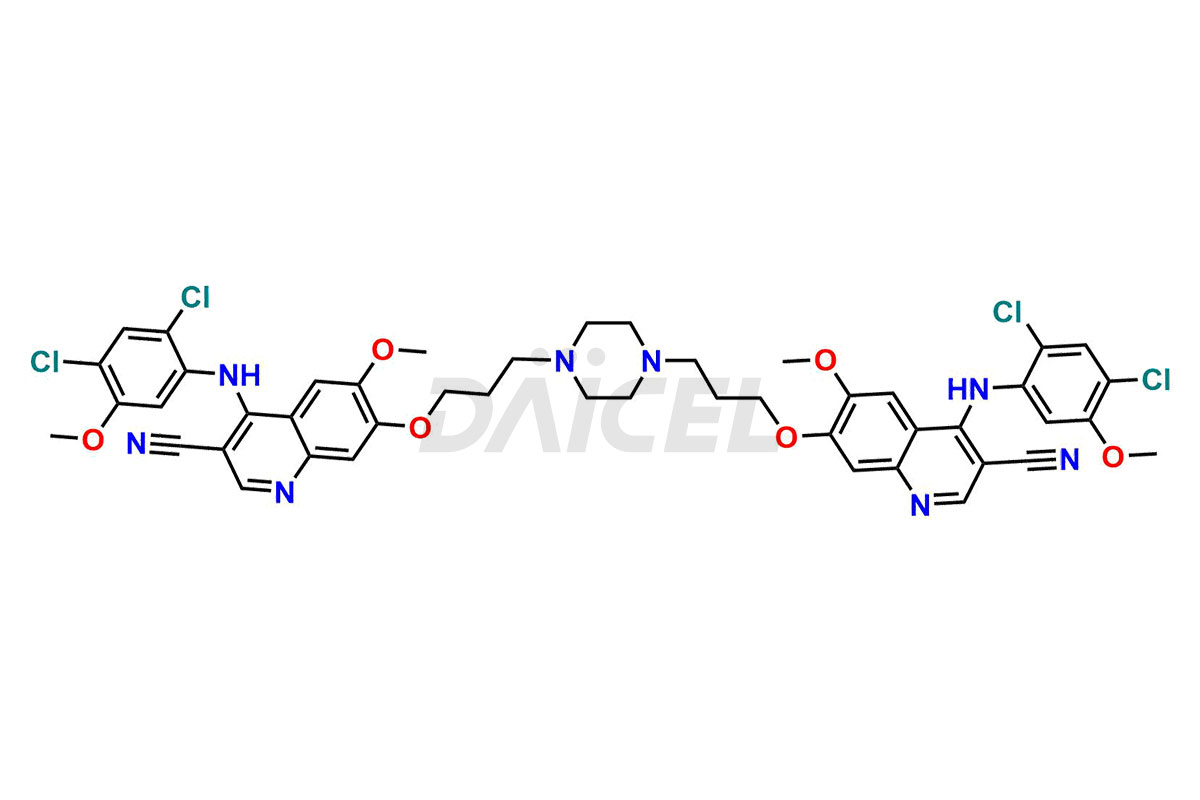
Daicel Pharma synthétise des impuretés de bosutinib d'une qualité exceptionnelle, telles que l'impureté de bosutinib-I, l'impureté de bosutinib-II, l'impureté de bosutinib-III, l'impureté de bosutinib-IV, l'impureté de bosutinib-V, l'impureté de bosutinib-VI et le bosutinib déchloré Oxy. Ces impuretés sont cruciales pour évaluer la pureté, la fiabilité et la sécurité du bosutinib, un ingrédient pharmaceutique actif. En outre, Daicel Pharma propose une synthèse personnalisée des impuretés du bosutinib pour répondre aux demandes de livraison des clients dans le monde entier.
Bosutinib [CAS : 380843/75/4] est un médicament destiné au traitement de la leucémie myéloïde chronique à chromosome Philadelphie positif chez les patients. Il s'agit d'un dérivé synthétique de quinolone et d'un double inhibiteur de kinase des tyrosine kinases BCR-ABL et Src. Le bosutinib peut potentiellement empêcher la croissance et la propagation des cellules cancéreuses en bloquant les enzymes.
Bosutinib : utilisation et disponibilité commerciale
Le bosutinib, sous la marque Bosulif, est un médicament approuvé pour le traitement des patients adultes diagnostiqués avec une leucémie myéloïde chronique (LMC Ph+) chronique, accélérée ou en phase blastique. Il aide à contrôler la croissance et la propagation des cellules leucémiques dans la LMC.
Structure et mécanisme d'action du bosutinib 
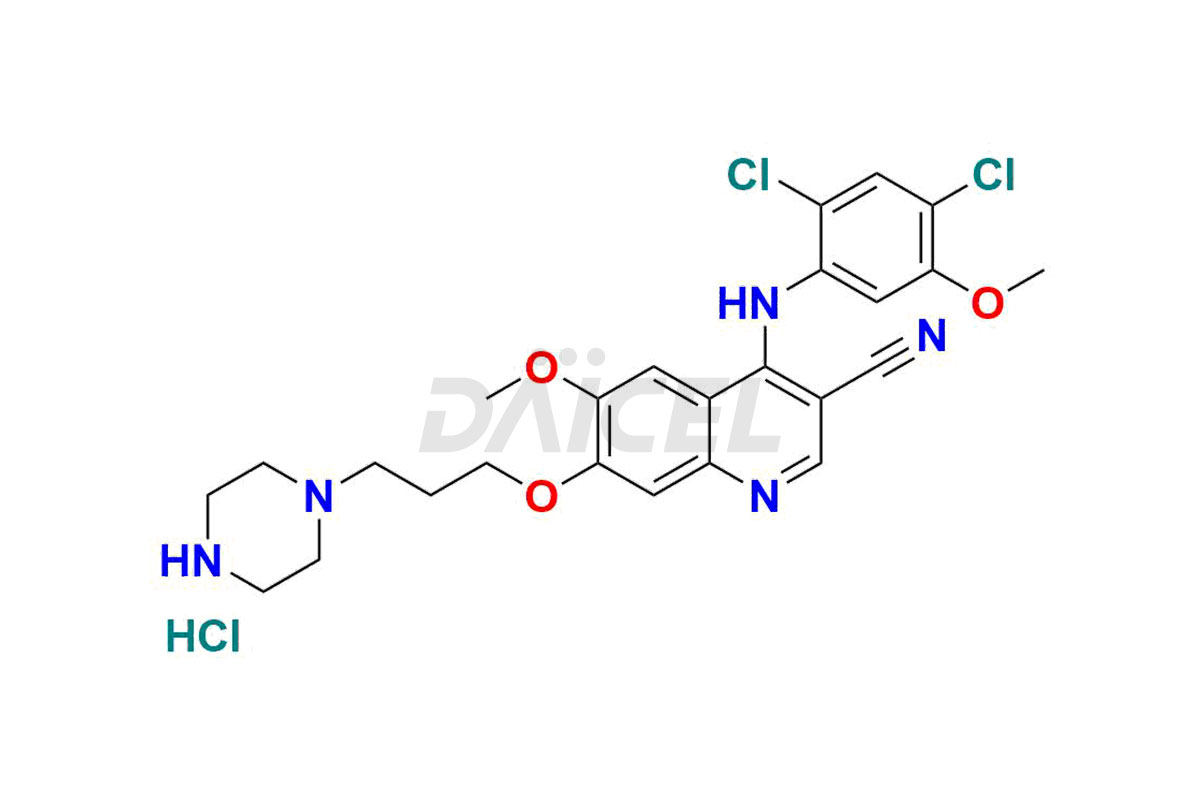
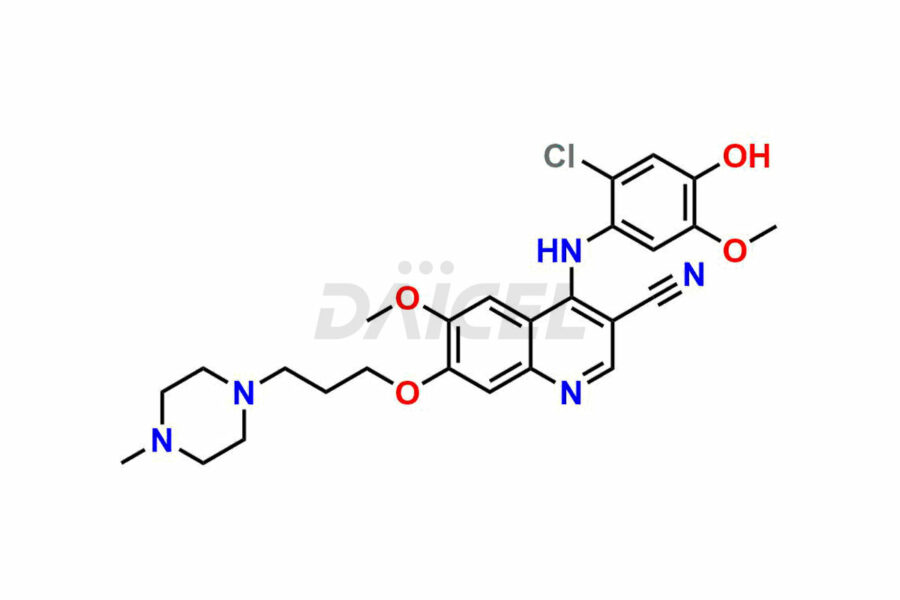
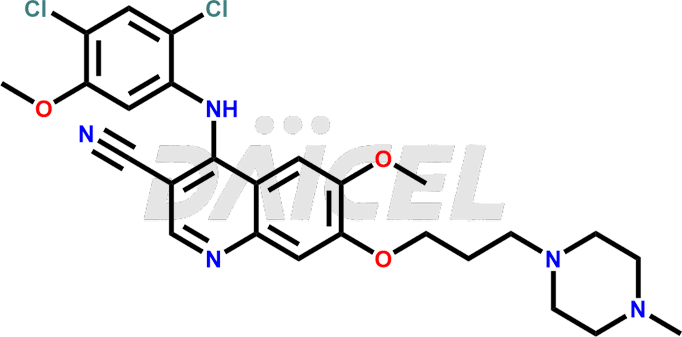
Le nom chimique du bosutinib est 4-[(2,4-dichloro-5-méthoxyphényl)amino]-6-méthoxy-7-[3-(4-méthyl-1-pipérazinyl)propoxy]-3-quinoléinecarbonitrile. Sa formule chimique est C26H29Cl2N5O3, et son poids moléculaire est d'environ 530.4 g/mol.
Le bosutinib inhibe la kinase Bcr-Abl et les kinases de la famille Src. Il inhibe 16 des 18 formes de Bcr-Abl résistantes à l'imatinib exprimées dans les lignées cellulaires myéloïdes murines.
Impuretés et synthèse du bosutinib
Les impuretés du bosutinib sont organiques ou inorganiques, liées au procédé ou au médicament. Des impuretés organiques peuvent se former lors de la synthèse1, la dégradation ou le stockage de la substance médicamenteuse, tandis que des impuretés inorganiques sont générées lors de la fabrication. Ils peuvent affecter la qualité et la stabilité du médicament, leurs niveaux doivent donc être contrôlés et minimisés lors de la synthèse.
Daicel Pharma propose un certificat d'analyse (CoA) pour les étalons d'impuretés du bosutinib, tels que l'impureté du bosutinib-I, l'impureté du bosutinib-II, l'impureté du bosutinib-III, l'impureté du bosutinib-IV, l'impureté du bosutinib-V, l'impureté du bosutinib-VI et Oxy déchloré. Bosutinib, généré à partir d'une installation d'analyse conforme aux normes cGMP. Le CoA comprend un rapport de caractérisation complet comprenant des données provenant de techniques telles que la RMN 1H, la RMN 13C, l'IR, la MASS et la pureté HPLC.2. De plus, sur demande, nous pouvons fournir des données supplémentaires telles que 13C-DEPT et CHN. Daicel Pharma peut préparer des impuretés ou des produits de dégradation inconnus du bosutinib. Un rapport de caractérisation complet accompagne chaque livraison.
Bibliographie
FAQ
Bibliographie
- Boschelli, Diane Harris ; Wang, Yanong Daniel ; Johnson, Steve Lawrence ; Berger, Dan Maarten, Processus de préparation de 7-substitués-3 quinolinecarbonitriles, Wyeth Holdings Corporation, États-Unis, US6780996B2, 24 août 2004
- Chaudhari, Vidya L. ; Kulkarni, Amol A., Méthode RP-HPLC pour l'estimation du Bosutinib sous forme en vrac selon les directives de l'ICH, World Journal of Pharmaceutical Research, Volume : 5, Numéro : 12, Pages : 417-424, 2016
Foire aux Questions
Pourquoi est-il essentiel de contrôler les impuretés du Bosutinib ?
Le contrôle des impuretés contenues dans le bosutinib est essentiel car ils peuvent affecter la sécurité et l'efficacité des médicaments. Ils peuvent également provoquer des effets indésirables et avoir un impact sur la qualité du produit médicamenteux.
Comment les impuretés du bosutinib sont-elles contrôlées lors de la fabrication ?
Les impuretés du bosutinib sont contrôlées pendant la fabrication à l'aide de méthodes analytiques validées, en surveillant les conditions de réaction et en mettant en œuvre des mesures de contrôle qualité.
Toutes les impuretés du bosutinib peuvent-elles être éliminées ?
Il se peut qu'il ne soit pas possible d'éliminer toutes les impuretés du Bosutinib. Cependant, leur contrôle se situe dans des limites acceptables grâce à des processus de fabrication et de contrôle qualité rigoureux.
Quelles sont les conditions de température requises pour conserver les impuretés du bosutinib ?
Les impuretés du bosutinib sont conservées à une température ambiante contrôlée entre 2 et 8 °C ou comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.