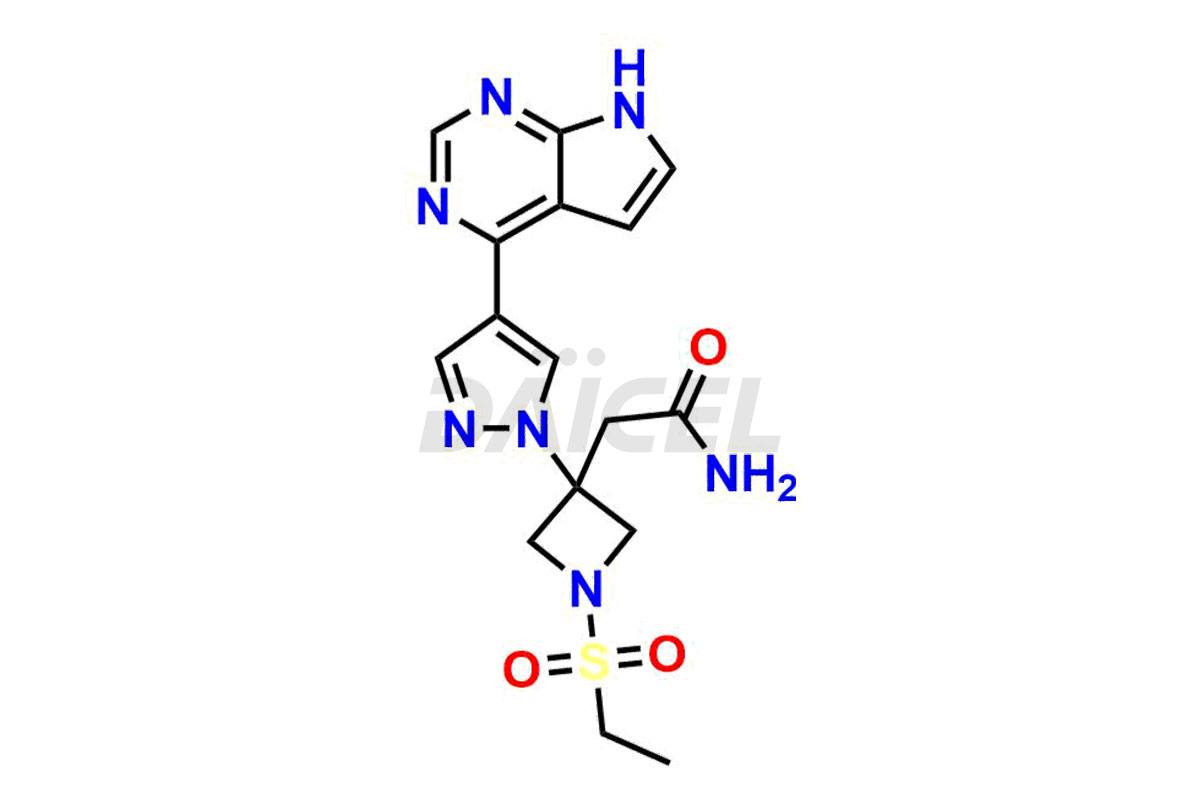
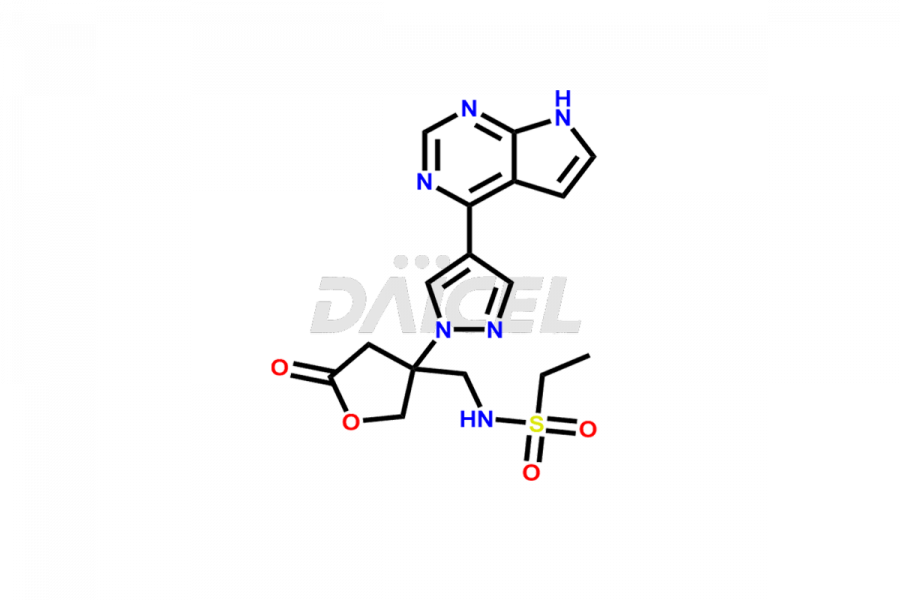
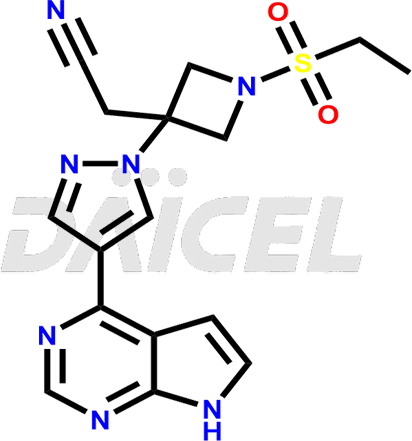
Baricitinib
Renseignements généraux
Impuretés du baricitinib et baricitinib
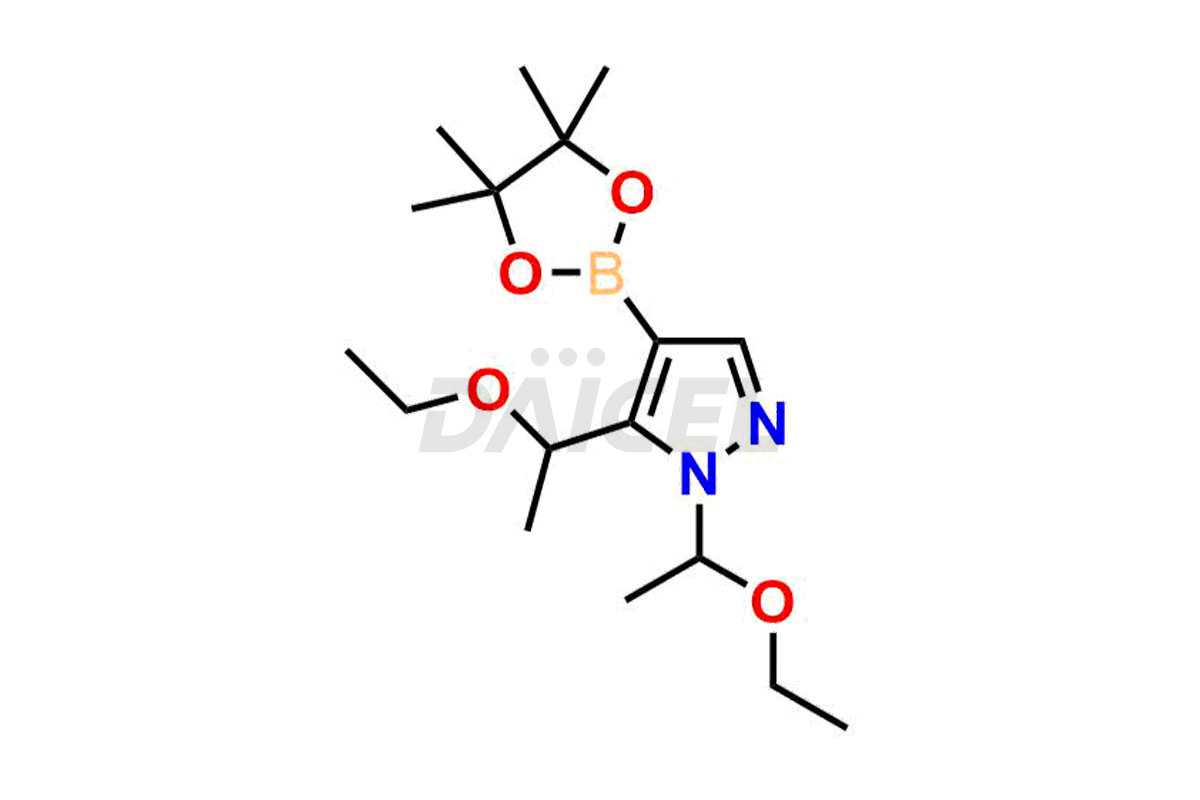
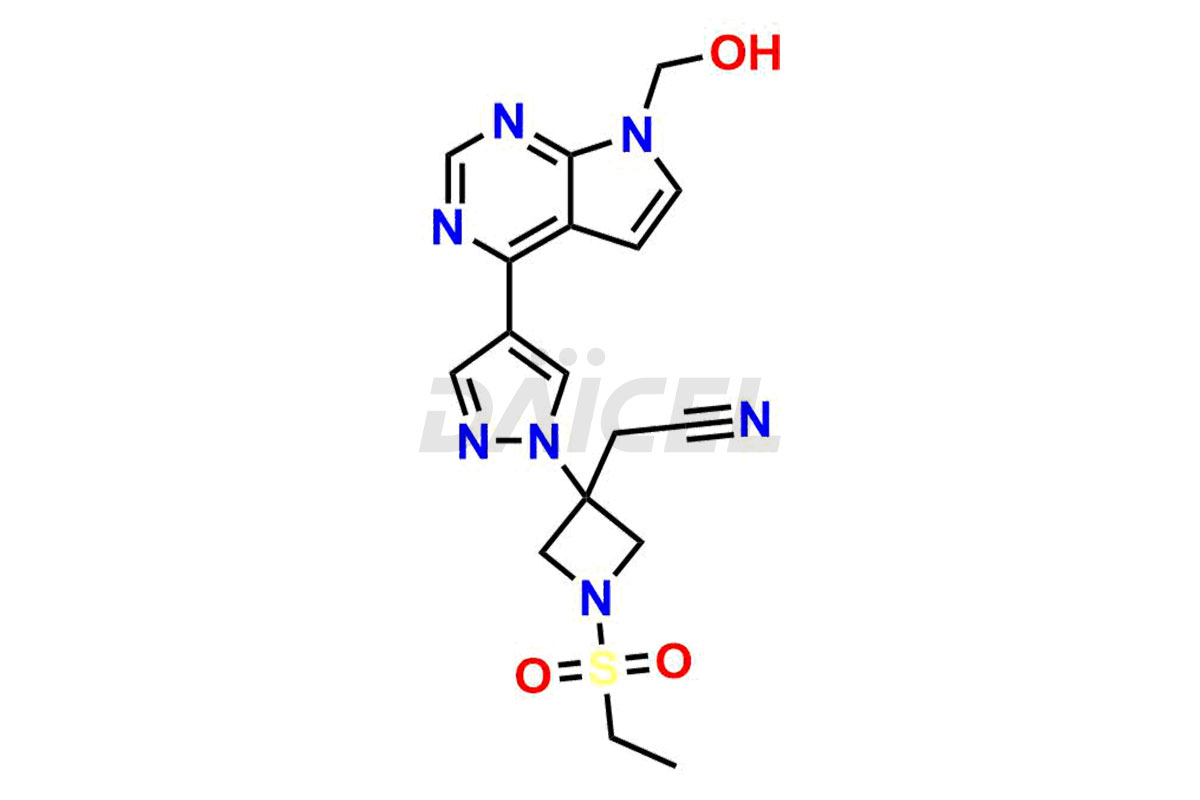
Daicel Pharma synthétise des impuretés de baricitinib de haute qualité, notamment 2-(1-(ethylsulfonyl)-3-(4-(7-(hydroxymethyl)-7H-pyrrolo[2,3-d]pyrimidin-4-yl)-1H-pyrazol-1-yl)azetidin-3-yl)acetonitrile, Baricitinib Acid Impurity, Baricitinib Amide Impurity, N-((3-(4-(7H-pyrrolo[2,3-d]pyrimidin-4-yl)-1H-pyrazol-1-yl)-5-oxotetrahydrofuran-3-yl)methyl) ethanesulfonamide, 2-(1-(ethylsulfonyl)-3-(4-(7-((2-(trimethylsilyl)ethoxy)methyl)-7H-pyrrolo[2,3-d]pyrimidin-4-yl)-1H-pyrazol-1-yl)azetidin-3-yl) acetonitrile, and so on. Ces impuretés sont essentielles pour évaluer la qualité, la stabilité et la sécurité du Baricitinib, un ingrédient pharmaceutique actif. De plus, Daicel Pharma propose une synthèse personnalisée d'impuretés de baricitinib pour une livraison mondiale afin de répondre aux besoins spécifiques de nos clients.
Baricitinib [CAS : 1187594/09/7] est un inhibiteur de la Janus kinase (JAK) à petite molécule. Il traite la polyarthrite rhumatoïde modérée à sévère, la pelade et le COVID-19 sévère chez les patients hospitalisés nécessitant une supplémentation en oxygène. Le baricitinib réduit l’inflammation, module le système immunitaire et possède des propriétés antinéoplasiques.
Baricitinib : utilisation et disponibilité commerciale
Le baricitinib est un médicament antirhumatismal approuvé par la FDA des États-Unis pour une utilisation chez les adultes atteints de polyarthrite rhumatoïde modérément à sévèrement active qui n'ont pas répondu de manière adéquate à d'autres médicaments antirhumatismaux de fond, tels que les traitements anti-TNF. Le baricitinib est disponible sous le nom commercial Olumiant.
Structure et mécanisme d'action du baricitinib 
Le nom chimique du baricitinib est 1-(éthylsulfonyl)-3-[4-(7H-pyrrolo[2,3-d]pyrimidin-4-yl)-1H-pyrazol-1-yl]-3-azétidine acétonitrile. Sa formule chimique est C16H17N7O2S, et son poids moléculaire est d'environ 371.4 g/mol.
Le baricitinib inhibe les Janus kinases, des enzymes qui transmettent les signaux des interactions cytokines ou facteur de croissance-récepteur sur les membranes cellulaires.
Impuretés et synthèse du baricitinib
Pendant la fabrication1 du baricitinib, des impuretés peuvent se former dans la substance médicamenteuse, ce qui peut affecter sa sécurité et son efficacité. Certaines impuretés courantes du baricitinib comprennent des composés apparentés, des dégradants et des solvants résiduels. Il est donc essentiel de les contrôler et de garantir la pureté de la substance médicamenteuse.
Daicel Pharma fournit un certificat d'analyse (CoA) pour les étalons d'impuretés du baricitinib, y compris 2-(1-(ethylsulfonyl)-3-(4-(7-(hydroxymethyl)-7H-pyrrolo[2,3-d]pyrimidin-4-yl)-1H-pyrazol-1-yl)azetidin-3-yl)acetonitrile, Baricitinib Acid Impurity, Baricitinib Amide Impurity, N-((3-(4-(7H-pyrrolo[2,3-d]pyrimidin-4-yl)-1H-pyrazol-1-yl)-5-oxotetrahydrofuran-3-yl)methyl) ethanesulfonamide, 2-(1-(ethylsulfonyl)-3-(4-(7-((2-(trimethylsilyl)ethoxy)methyl)-7H-pyrrolo[2,3-d]pyrimidin-4-yl)-1H-pyrazol-1-yl)azetidin-3-yl) acetonitrile, and so on. Le CoA est généré à partir d'une installation d'analyse conforme aux BPF et comprend des données de caractérisation complètes telles que la RMN 1H, la RMN 13C, l'IR, la MASS et la pureté HPLC. Nous pouvons également fournir des données de caractérisation supplémentaires comme 13C-DEPT et CHN sur demande. Daicel Pharma est capable de créer des impuretés ou des produits de dégradation inconnus du baricitinib. Chaque livraison dispose d'un rapport de caractérisation complet.
Bibliographie
FAQ
Bibliographie
- Rodgers, James D. ; Shepard, Stacey ; Li, Yun-Long ; Zhou, Jiacheng ; Liu, Pingli ; Meloni, David; Xia, Michael, dérivés d'azétidine et de cyclobutane comme inhibiteurs de JAK, Incyte Corporation, États-Unis, US8158616B2, 17 avril 2012
- Gandhi, Santosh V. ; Kapoor, Barkha G., Développement et validation d'une méthode spectroscopique UV pour l'estimation du baricitinib, Journal of Drug Delivery and Therapeutics, Volume : 9, Numéro : 4Suppl., Pages : 488-491, 2019
Foire aux Questions
Comment les impuretés du baricitinib sont-elles contrôlées pendant le processus de fabrication du médicament ?
Les impuretés du Baricitinib sont contrôlées pendant la fabrication en mettant en œuvre de bonnes pratiques de fabrication (BPF), telles que l'utilisation de matières premières de haute qualité et l'emploi de techniques de purification appropriées.
Les impuretés du baricitinib peuvent-elles affecter la stabilité du produit médicamenteux ?
Oui, les impuretés contenues dans le Baricitinib peuvent affecter la stabilité du produit médicamenteux, entraînant une dégradation et une diminution de son efficacité.
Existe-t-il des méthodes spécifiques pour contrôler les impuretés présentes dans le baricitinib ?
Oui, les méthodes spécifiques de contrôle des impuretés contenues dans le baricitinib dépendent du type d’impureté et de sa source. Par exemple, le contrôle des impuretés liées aux procédés implique l’optimisation des procédés de synthèse et l’utilisation de techniques de purification appropriées.
Quelles sont les conditions de température requises pour stocker les impuretés du baricitinib ?
Les impuretés du baricitinib sont conservées à une température ambiante contrôlée entre 2 et 8 °C ou comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.

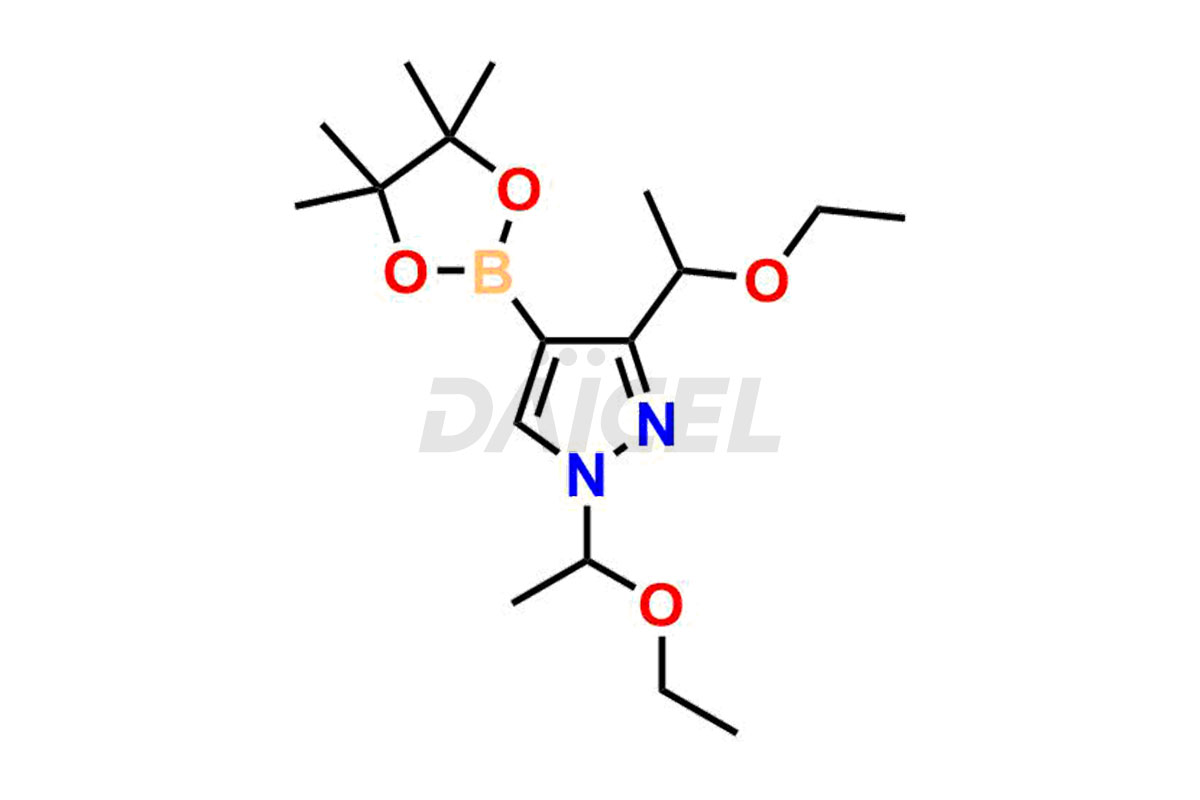

![4-(1H-pyrazol-4-yl)-7H-pyrrolo[2,3-d]pyrimidine | Normes pharmaceutiques Daicel](https://d8ekk6dtachh7.cloudfront.net/wp-content/uploads/2022/06/DCTI-C-1824-900x600.jpg)