Amphotéricine
Renseignements généraux
Impuretés d'amphotéricine et amphotéricine
Daicel Pharma synthétise des impuretés d'amphotéricine de haute qualité, notamment l'impureté B de l'amphotéricine B EP et l'impureté C de l'amphotéricine B EP. Ces impuretés sont essentielles pour évaluer la qualité, la stabilité et la sécurité de l'amphotéricine, qui est un ingrédient pharmaceutique actif. De plus, Daicel Pharma propose une synthèse personnalisée d'impuretés d'amphotéricine avec une livraison mondiale pour répondre aux besoins spécifiques de nos clients.
Amphotéricine [CAS : 12633/72/6] ou amphotéricine B [C 1397/89/3] est un antibiotique antifongique de Streptomyces nodosus. Il traite les infections antifongiques et la leishmaniose.
Amphotéricine : utilisation et disponibilité commerciale
L'amphotéricine B est un médicament antifongique approuvé par la FDA américaine pour traiter plusieurs infections fongiques, notamment l'histoplasmose, la cryptococcose et la leishmaniose. L'amphotéricine B traite les infections fongiques invasives. La dose quotidienne recommandée dépend du type d'infection, de l'organe touché et du statut immunitaire du patient. Le médicament est disponible sous différentes marques, notamment Abelcet, Ambisome, Amphotec, Fungizone, etc.
Structure de l'amphotéricine et mécanisme d'action 
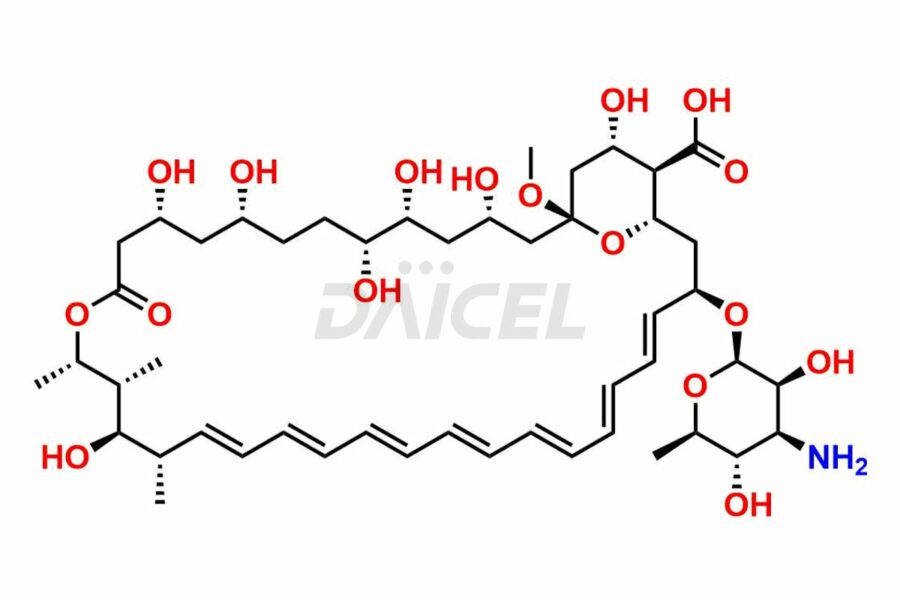
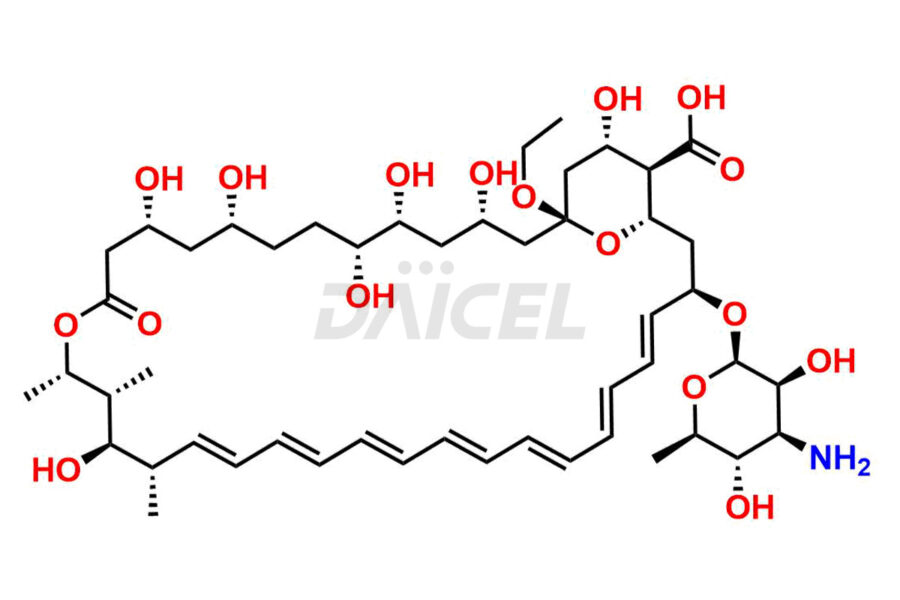
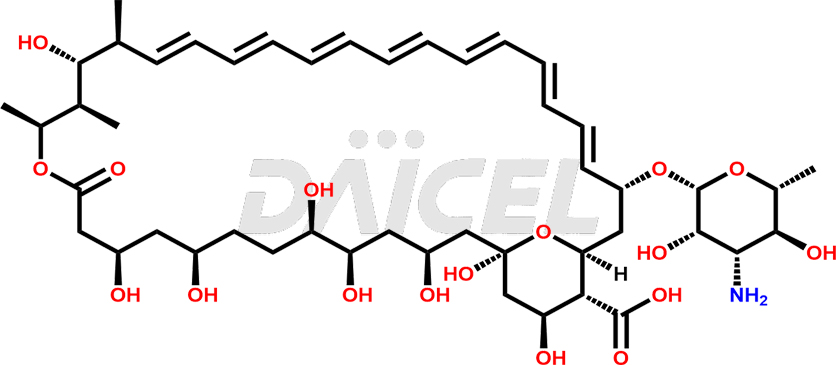
The chemical name of Amphotericin B is (1R,3S,5R,6R,9R,11R,15S,16R,17R,18S,19E,21E,23E,25E,27E,29E,31E,33R,35S,36R,37S)-33-[(3-Amino-3,6-dideoxy-β-D-mannopyranosyl)oxy]-1,3,5,6,9,11,17,37-octahydroxy-15,16,18-trimethyl-13-oxo-14,39-dioxabicyclo[33.3.1]nonatriaconta-19,21,23,25,27,29,31-heptaene-36-carboxylic acid. Its chemical formula is C47H73NON17 et son poids moléculaire est d'environ 924.1 g/mol.
L'amphotéricine se lie à l'ergostérol, essentiel à la membrane cellulaire fongique. Son interaction provoque des modifications de la membrane cellulaire, conduisant à la mort cellulaire.
Impuretés et synthèse de l'amphotéricine
Des impuretés d'amphotéricine se forment lors de la fabrication, du stockage ou par dégradation dans certaines conditions. Certaines impuretés de l'amphotéricine B comprennent des substances apparentées, des produits de dégradation et des solvants résiduels. Des substances apparentées se forment lors de la synthèse ou de l’isolement de l’amphotéricine B et peuvent être structurellement similaires au médicament. Des produits de dégradation se produisent lorsque l'amphotéricine B est exposée à la lumière, à la chaleur, à des conditions acides ou alcalines. Ces produits de dégradation peuvent être toxiques et affecter l’efficacité du médicament. Les solvants résiduels peuvent également être présents dans l’amphotéricine B en raison de la fabrication. Il est essentiel de contrôler les impuretés contenues dans l’amphotéricine, car elles peuvent avoir un impact sur la sécurité, l’efficacité et la qualité des médicaments.
Daicel Pharma fournit un certificat d'analyse (CoA) pour les étalons d'impuretés d'amphotéricine, y compris l'impureté B de l'amphotéricine B EP et l'impureté C de l'amphotéricine B EP. Le CoA provient d'un établissement d'analyse conforme aux BPF et comprend des données de caractérisation complètes.1 tels que la RMN 1H, la RMN 13C, l'IR, la MASS et la pureté HPLC2. Nous pouvons également fournir des données de caractérisation supplémentaires comme 13C-DEPT et CHN sur demande. Daicel Pharma est capable de créer des impuretés ou des produits de dégradation inconnus de l'amphotéricine. Chaque livraison est accompagnée d'un rapport de caractérisation complet.
Bibliographie
FAQ
Bibliographie
- Gallelli, Joseph F., Dosage et stabilité de l'amphotéricine B dans des solutions aqueuses, Drug Intelligence, Volume : 1, Numéro : 3, Pages : 102-5, 1967
- Nilsson-Ehle, Ingrid ; Yoshikawa, Thomas T. ; Edwards, John E. ; Schotz, Michael C. ; Guze, Lucien B., Quantification de l'amphotéricine B par chromatographie liquide à haute pression, Journal of Infectious Diseases, Volume : 135, Numéro : 3, Pages : 414-22, 1977
Foire aux Questions
Comment la pureté de l’amphotéricine est-elle évaluée ?
La pureté de l'amphotéricine est évaluée à l'aide de techniques analytiques telles que la chromatographie liquide haute performance (HPLC), la chromatographie liquide-spectrométrie de masse (LC-MS), etc.
Quelle est l’importance de la validation des méthodes analytiques pour les tests d’impuretés dans l’amphotéricine ?
La validation des méthodes analytiques pour les tests d'impuretés dans l'amphotéricine est essentielle pour garantir son exactitude, sa précision, sa spécificité et sa sensibilité.
Les impuretés de l’amphotéricine peuvent-elles être éliminées par purification ?
Les méthodes de purification telles que la chromatographie, la filtration et la cristallisation aident à éliminer les impuretés de l'amphotéricine.
Quelles sont les conditions de température requises pour stocker les impuretés de l’amphotéricine ?
Les impuretés d'amphotéricine sont conservées à une température ambiante contrôlée entre 2 et 8 °C ou comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.