abacavir
Renseignements généraux
Impuretés de l'abacavir et abacavir
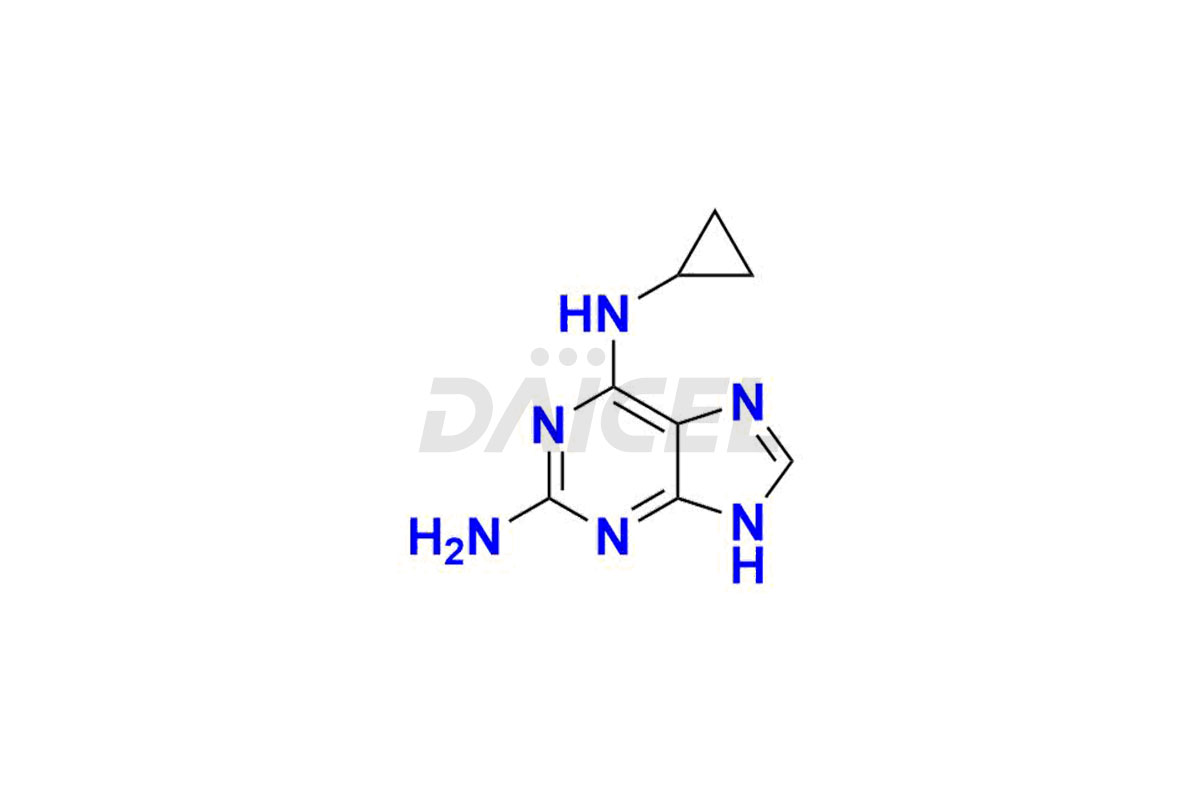
Daicel Pharma synthétise l'impureté Abacavir de haute qualité, la N6-Cyclopropyl-9H-Purin-2,6-diamine, qui est cruciale dans l'analyse de la qualité, de la stabilité et de la sécurité biologique de l'ingrédient pharmaceutique actif Abacavir. De plus, Daicel Pharma propose une synthèse personnalisée des impuretés de l'Abacavir et les livre dans le monde entier.
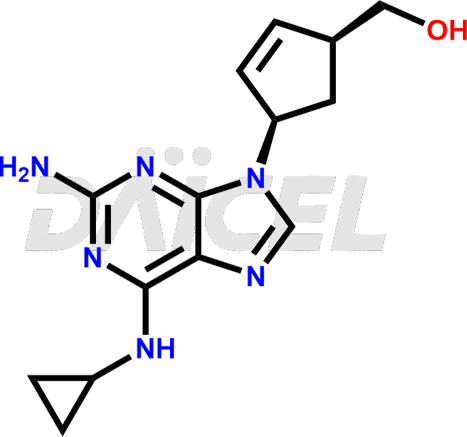
abacavir [CAS : 136470/78/5] est un analogue nucléosidique carbocyclique synthétique traitant l'infection par le VIH chez les adultes, les enfants et les nourrissons. Il se combine avec d'autres médicaments contre le VIH, en particulier le sulfate et d'autres médicaments antirétroviraux. L'abacavir agit comme un inhibiteur nucléosidique de la transcriptase inverse (INTI), qui aide à combattre le VIH en inhibant l'activité de l'enzyme transcriptase inverse du VIH-1 nécessaire à la réplication du virus.
Abacavir : utilisation et disponibilité commerciale
L'abacavir est un médicament approuvé par la FDA pour traiter l'infection par le VIH-1. Il est utilisé en association avec d'autres médicaments antirétroviraux, tels que l'abacavir/lamivudine/zidovudine, l'abacavir/dolutégravir/lamivudine et l'abacavir/lamivudine. L'abacavir est classé comme un inhibiteur nucléosidique de la transcriptase inverse (INTI) et peut être administré par voie orale sous forme de comprimé ou de solution. Les noms commerciaux de l'Abacavir incluent Epzicom (combinaison Abacavir-Lamivudine), Triumeq (combinaison Abacavir-Lamivudine-Dolutegravir), Trizivir (combinaison Abacavir-Lamivudine-Zidovudine) et Ziagen.
Structure de l'abacavir et mécanisme d'action 
Le nom chimique de l'abacavir est (1S,4R)-4-[2-Amino-6-(cyclopropylamino)-9H-purin-9-yl]-2-cyclopentène-1-méthanol. Sa formule chimique est C14H18N6O, et son poids moléculaire est d'environ 286.33 g/mol.
L'abacavir est converti en son métabolite actif, le carbovir triphosphate. C'est un analogue du désoxyguanosine-5¢-triphosphate (dGTP). Il inhibe l'activité de la transcriptase inverse (RT) du VIH-1.
Impuretés et synthèse de l'abacavir
Les impuretés de l'abacavir peuvent être classées en fonction des matières premières, du processus de réaction ou de la dégradation de la substance médicamenteuse. Les impuretés formées peuvent résulter du processus de synthèse1, les étapes de purification ou les conditions de stockage. Ils peuvent affecter la qualité, la sécurité et l’efficacité du médicament. Une surveillance et une analyse régulières permettent de garantir que les niveaux d'impuretés restent dans des limites acceptables et ne présentent pas de risque pour les patients.
Daicel fournit un certificat d'analyse (CoA) pour l'étalon d'impureté Abacavir, N6-Cyclopropyl-9H-Purin-2,6-diamine. Le CoA est émis par une installation d'analyse conforme aux BPF et contient des données de caractérisation complètes, telles que la RMN 1H, la RMN 13C, l'IR, la MASS et la pureté HPLC.2. Des données de caractérisation supplémentaires, telles que 13C-DEPT et CHN, peuvent être fournies sur demande. Daicel peut également préparer toute impureté ou produit de dégradation inconnu de l’Abacavir. Nous remettons un rapport de caractérisation complet à la livraison.
Bibliographie
- Daluge, Susan Mary, Nucléosides thérapeutiques, Wellcome Foundation Ltd., Royaume-Uni, US5034394A, 23 juillet 1991
- Veldkamp, AI; Sparidans, RW ; Hötelmans, RMW ; Beijnen, JH, Détermination quantitative de l'abacavir (1592U89), un nouvel inhibiteur nucléosidique de la transcriptase inverse, dans le plasma humain par chromatographie liquide haute performance isocratique en phase inversée avec détection ultraviolette, Journal of Chromatography B : Biomedical Sciences and Applications, Volume : 736, Numéro : 1 + 2, Pages : 123-128, 1999
Foire aux Questions
Quelle est la source des impuretés de l’Abacavir ?
La source d'impuretés de l'abacavir peut inclure des matières premières, des solvants, des réactifs et des produits de dégradation formés lors de la fabrication ou du stockage du produit médicamenteux.
Comment les impuretés présentes dans l’Abacavir sont-elles détectées et quantifiées ?
Les impuretés de l'abacavir sont détectées et quantifiées à l'aide de techniques chromatographiques et spectroscopiques, telles que HPLC, UPLC et LC-MS.
Comment les impuretés de l’Abacavir sont-elles surveillées ?
Les impuretés de l'abacavir sont surveillées par des tests réguliers de la substance médicamenteuse et du produit pendant la fabrication et tout au long de sa durée de conservation.
Quelles sont les conditions de température nécessaires pour stocker les impuretés de l’Abacavir ?
Les impuretés de l'abacavir sont conservées à une température ambiante contrôlée entre 2 et 8 ⁰C ou comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.