Φαβιπιραβίρη
Γενικές πληροφορίες
Προσμίξεις Favipiravir και Favipiravir
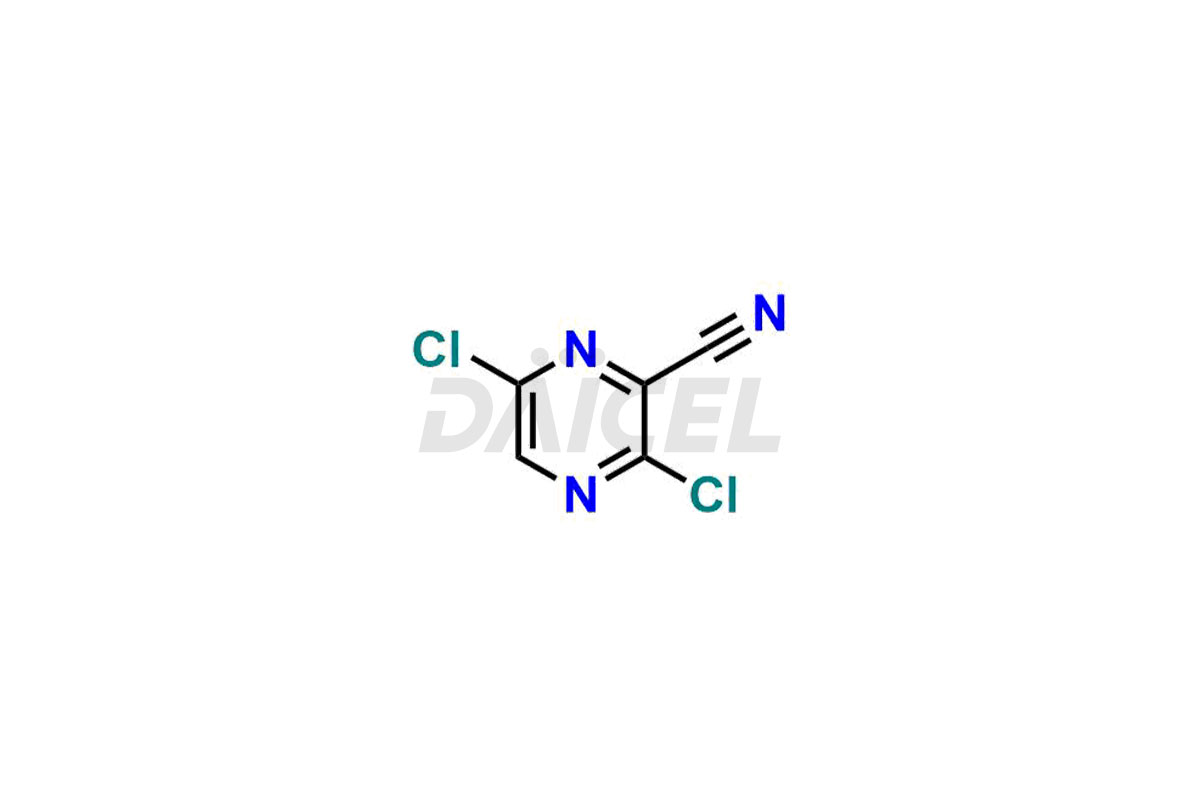
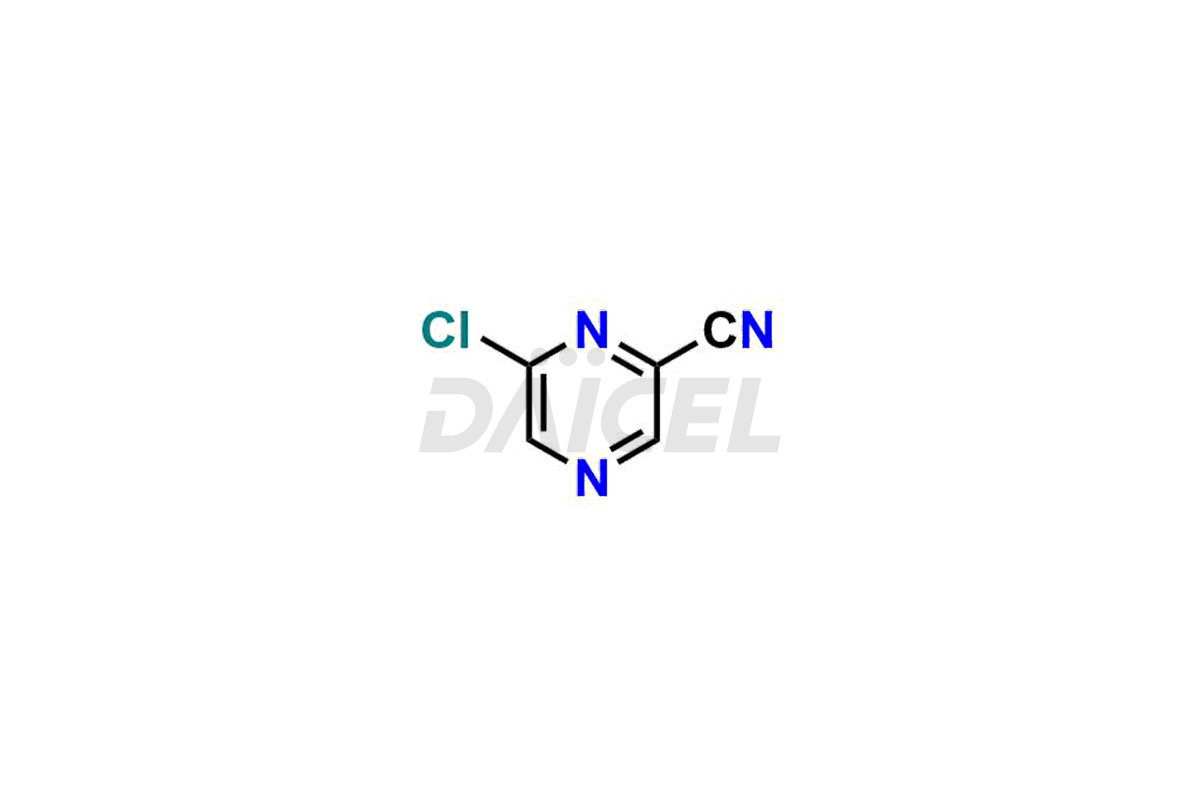
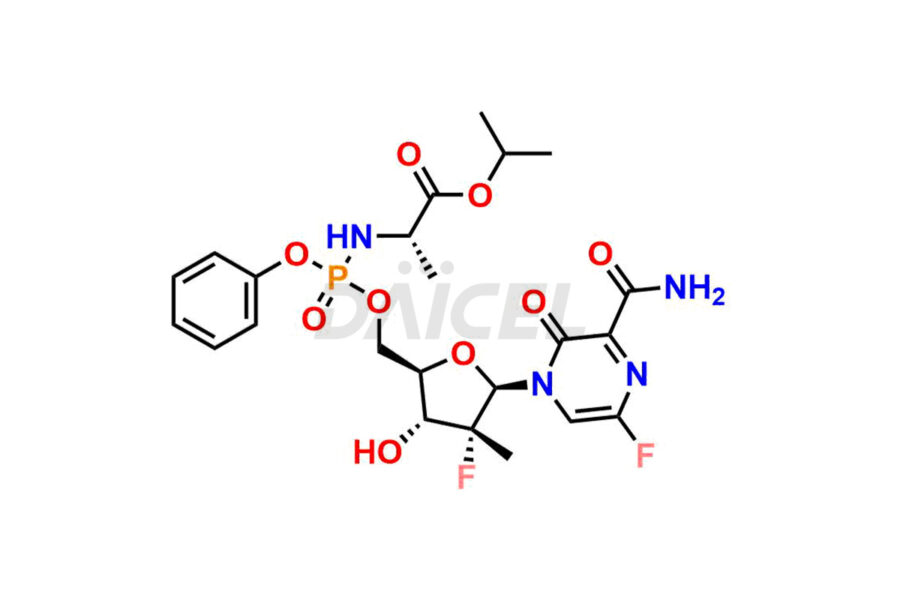
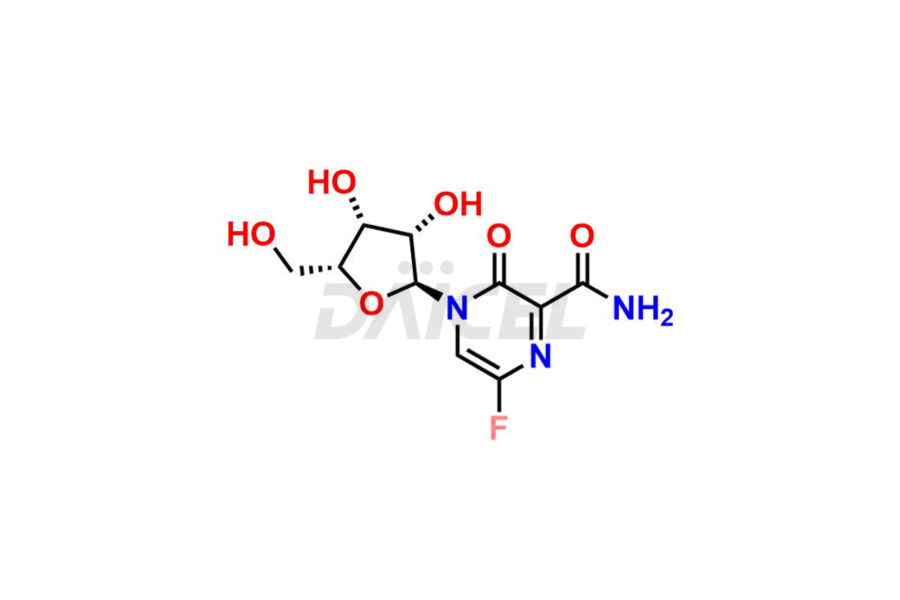
Ντάικελ Η Pharma προσφέρει ακαθαρσίες υψηλής ποιότητας για το Favipiravir, ένα ενεργό φαρμακευτικό συστατικό. Αυτές οι ακαθαρσίες, συμπεριλαμβανομένων των 3-υδροξυπυραζινο-2-καρβοξαμιδίου, 3,6-διχλωροπυραζινο-2-καρβονιτριλίου, 6-βρωμο-3-υδροξυπυραζινο-2-καρβοξαμιδίου, 6-χλωρο-3-υδροξυπυραζινο-2-καρβοξαμιδίου, 6-χλωροϋπυραζίνης Το 2-καρβονιτρίλιο, το Favipiravir fluoro Ribofuranose, το Favipiravir Ribofuranose και ο Favipiravir Ribofuranose μεταβολίτης, διαδραματίζουν ζωτικό ρόλο στην αξιολόγηση της καθαρότητας, της αξιοπιστίας και της ασφάλειας του Favipiravir. Η Daicel Pharma προσφέρει επίσης μια προσαρμοσμένη σύνθεση ακαθαρσιών Favipiravir για να καλύψει τις απαιτήσεις των πελατών, με διαθέσιμες επιλογές παράδοσης σε όλο τον κόσμο.
Φαβιπιραβίρη [CAS: 259793-96-9] είναι ένα αντιικό φάρμακο που είναι παράγωγο πυραζινοκαρβοξαμιδίου. Επιδεικνύει δράση έναντι των ιών RNA αναστέλλοντας επιλεκτικά την εξαρτώμενη από RNA πολυμεράση RNA των ιών RNA. Το Favipiravir θεραπεύει τη γρίπη και είναι ένας αντιιικός παράγοντας και ένας κατευθυνόμενος από το RNA αναστολέας της RNA πολυμεράσης. Επιπλέον, βοηθά στην καταπολέμηση του κορωνοϊού.
Favipiravir: Χρήση και Εμπορική Διαθεσιμότητα
Το Favipiravir, γνωστό με την επωνυμία Avigan, εγκρίθηκε αρχικά στην Ιαπωνία το 2014 για τη θεραπεία περιπτώσεων γρίπης που δεν ανταποκρίνονταν στις συμβατικές θεραπείες. Η αποτελεσματικότητά του στη στόχευση διαφόρων στελεχών της γρίπης έχει προκαλέσει έρευνες για την πιθανή χρήση του έναντι άλλων ιογενών λοιμώξεων, συμπεριλαμβανομένων του Έμπολα και του COVID-19. Το Favipiravir δρα ως ανάλογο πουρίνης, υποκαθιστώντας τη γουανίνη ή την αδενίνη κατά τη διάρκεια της ιικής αντιγραφής, εμποδίζοντας έτσι τη διαδικασία αντιγραφής. Μπορεί να θεραπεύσει απειλητικές για τη ζωή λοιμώξεις όπως ο Έμπολα, ο πυρετός Lassa και η λύσσα, καθιερώνοντας τη θεραπευτική του αξία σε αυτές τις ασθένειες.
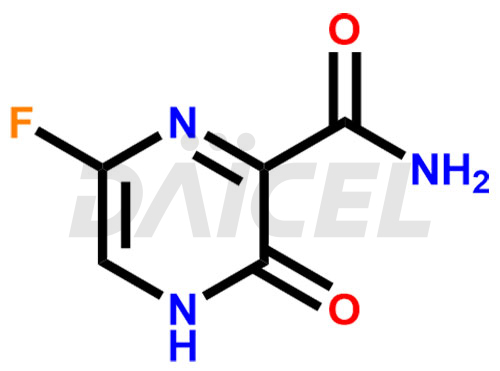
Δομή και μηχανισμός δράσης του Favipiravir 
Η χημική ονομασία του Favipiravir είναι 6-Fluoro-3,4-dihydro-3-oxo-2-pyrazinecarboxamide. Ο χημικός του τύπος είναι C5H4FN3O2, και το μοριακό του βάρος είναι περίπου 157.10 g/mol.
Η φαβιπιραβίρη αναστέλλει εκλεκτικά την πολυμεράση RNA που εξαρτάται από το RNA του ιού της γρίπης.
Προσμείξεις και σύνθεση Favipiravir
Οι ακαθαρσίες στο Favipiravir αναφέρονται σε ανεπιθύμητες ουσίες ή υποπροϊόντα που υπάρχουν στο φάρμακο. Μπορούν να προκύψουν κατά τη διάρκεια της σύνθεσης1, διαδικασίες παραγωγής ή αποθήκευσης. Περιλαμβάνουν σχετικές ενώσεις, προϊόντα αποδόμησης, υπολειμματικούς διαλύτες ή άλλες ακαθαρσίες που εισάγονται κατά την παραγωγή ή το χειρισμό. Μπορούν να επηρεάσουν την καθαρότητα, τη σταθερότητα και τη συνολική ποιότητα του Favipiravir. Οι αυστηρές ρυθμιστικές οδηγίες και τα μέτρα ποιοτικού ελέγχου βοηθούν στην παρακολούθηση και τον έλεγχο των επιπέδων ακαθαρσιών για να διασφαλιστεί η ασφάλεια και η αποτελεσματικότητα των φαρμάκων Favipiravir. Είναι σημαντικό να ελαχιστοποιηθούν και να διαχειρίζονται για να διατηρηθεί η ακεραιότητα και η θεραπευτική αξία του Favipiravir.
Η Daicel Pharma προσφέρει ένα ολοκληρωμένο Πιστοποιητικό Ανάλυσης (CoA) για τα πρότυπα ακαθαρσίας Favipiravir, συμπεριλαμβανομένων των 3-υδροξυπυραζινο-2-καρβοξαμίδη, 3,6-διχλωροπυραζίνη-2-καρβονιτρίλιο, 6-βρωμο-3-υδροξυπυραζίνη-2-καρβοξαμίδιο, 6-Χρβοξαμίδιο -3-υδροξυπυραζινο-2-καρβοξαμίδιο, 6-χλωροϋπυραζινο-2-καρβονιτρίλιο, Favipiravir fluoro Ribofuranose, Favipiravir Ribofuranose και Favipiravir Ribofuranose μεταβολίτης. Παράγουν από μια αναλυτική εγκατάσταση που συμμορφώνεται με τα πρότυπα cGMP. Το CoA παρέχει μια λεπτομερή αναφορά χαρακτηρισμού με δεδομένα που λαμβάνονται μέσω τεχνικών όπως η ανάλυση καθαρότητας 1H NMR, 13C NMR, IR, MASS και HPLC2. Παρέχουμε πρόσθετα δεδομένα όπως 13C-DEPT κατόπιν αιτήματος. Η Daicel Pharma συνθέτει άγνωστες προσμίξεις Favipiravir ή προϊόντα αποδόμησης. Κάθε παράδοση έχει μια πλήρη αναφορά χαρακτηρισμού.
αναφορές
Συχνές Ερωτήσεις
αναφορές
- Furuta, Yousuke; Egawa, Hiroyuki, αζωτούχα ετεροκυκλικά παράγωγα καρβοξαμιδίου ή άλας τους ως αντιιικοί παράγοντες, Toyama Chemical Co., Ltd., Ιαπωνία, EP1112743B1, 24 Οκτωβρίου 2007 (https://patents.google.com/patent/EP1112743B1/en)
- Bulduk, Ibrahim, μέθοδος HPLC-UV για ποσοτικοποίηση της φαβιπιραβίρης σε φαρμακευτικά σκευάσματα, Acta Chromatographica, Τόμος: 33, Τεύχος: 3, Σελίδες: 209-215, 2021
Συχνές Ερωτήσεις
Πώς χαρακτηρίζονται οι ακαθαρσίες Favipiravir σε σκευάσματα φαρμάκων;
Διάφορες τεχνικές φυσικοχημικού χαρακτηρισμού, όπως ο προσδιορισμός του σημείου τήξης, οι μελέτες διαλυτότητας και η φασματοσκοπική ανάλυση, βοηθούν στον χαρακτηρισμό των ακαθαρσιών στα σκευάσματα Favipiravir.
Μπορούν οι ακαθαρσίες του Favipiravir στα σκευάσματα φαρμάκων να οδηγήσουν σε αλλαγές στις φαρμακοδυναμικές επιδράσεις του φαρμάκου;
Ορισμένες ακαθαρσίες στα σκευάσματα Favipiravir μπορεί να αλλάξουν τις φαρμακοδυναμικές επιδράσεις του φαρμάκου, επηρεάζοντας τον μηχανισμό δράσης του ή τα θεραπευτικά του αποτελέσματα.
Πώς ελέγχονται οι ακαθαρσίες του Favipiravir κατά την αποθήκευση και τη μεταφορά;
Οι κατάλληλες συνθήκες αποθήκευσης, όπως ο έλεγχος θερμοκρασίας και υγρασίας, και τα κατάλληλα υλικά συσκευασίας συμβάλλουν στην ελαχιστοποίηση του σχηματισμού ή της αποικοδόμησης ακαθαρσιών στο Favipiravir κατά την αποθήκευση και τη μεταφορά.
Πώς πρέπει να αποθηκεύονται οι ακαθαρσίες του Favipiravir όσον αφορά τη θερμοκρασία;
Οι προσμείξεις του Favipiravir αποθηκεύονται σε ελεγχόμενη θερμοκρασία δωματίου, 2-8 °C, ή σύμφωνα με τις προδιαγραφές του Πιστοποιητικού Ανάλυσης (CoA).
Σημείωση: Τα προϊόντα που προστατεύονται από έγκυρα διπλώματα ευρεσιτεχνίας από έναν κατασκευαστή δεν προσφέρονται προς πώληση σε χώρες που διαθέτουν προστασία ευρεσιτεχνίας. Η πώληση τέτοιων προϊόντων συνιστά παραβίαση διπλώματος ευρεσιτεχνίας και η ευθύνη της είναι με ευθύνη του αγοραστή.