Καβοτεγκραβίρη
Γενικές πληροφορίες
Προσμείξεις Cabotegravir και Cabotegravir
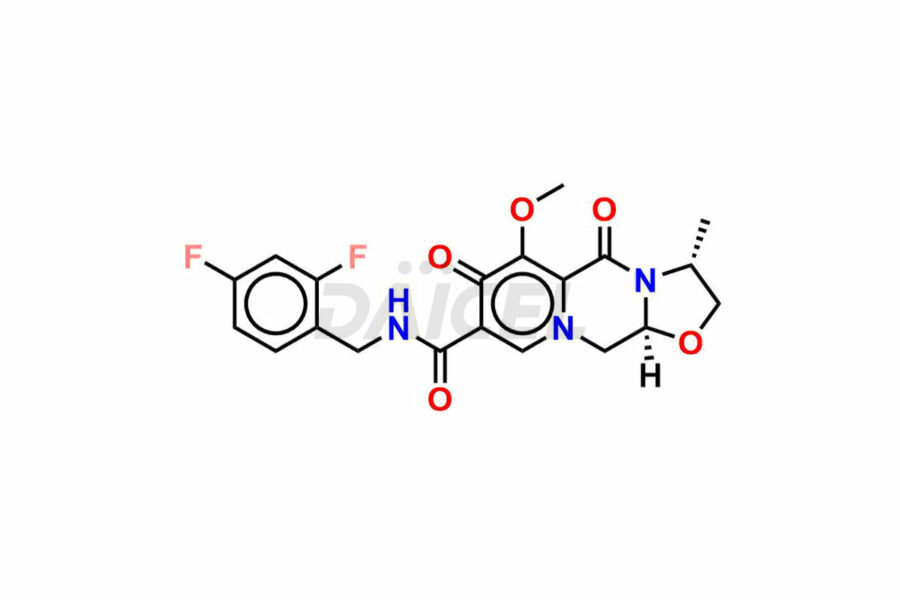
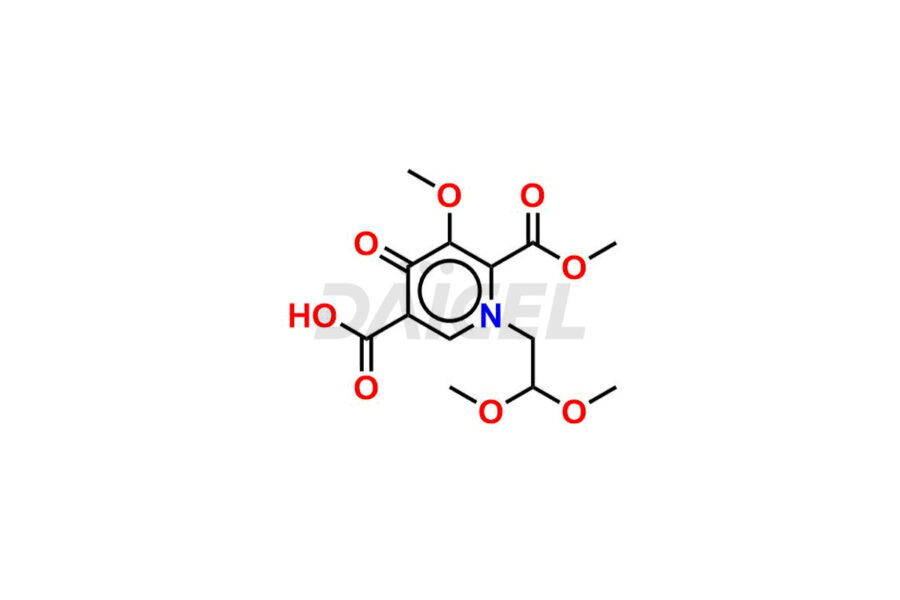
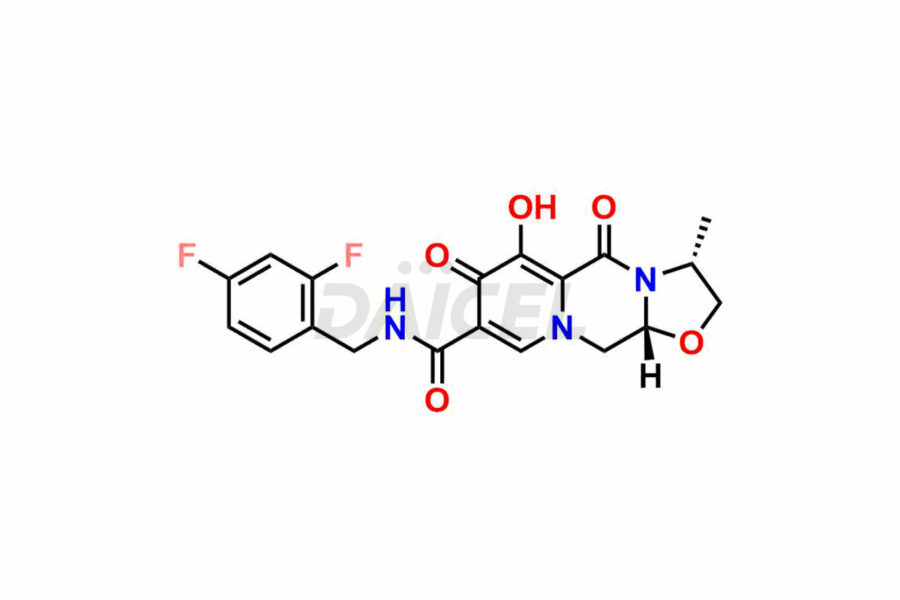
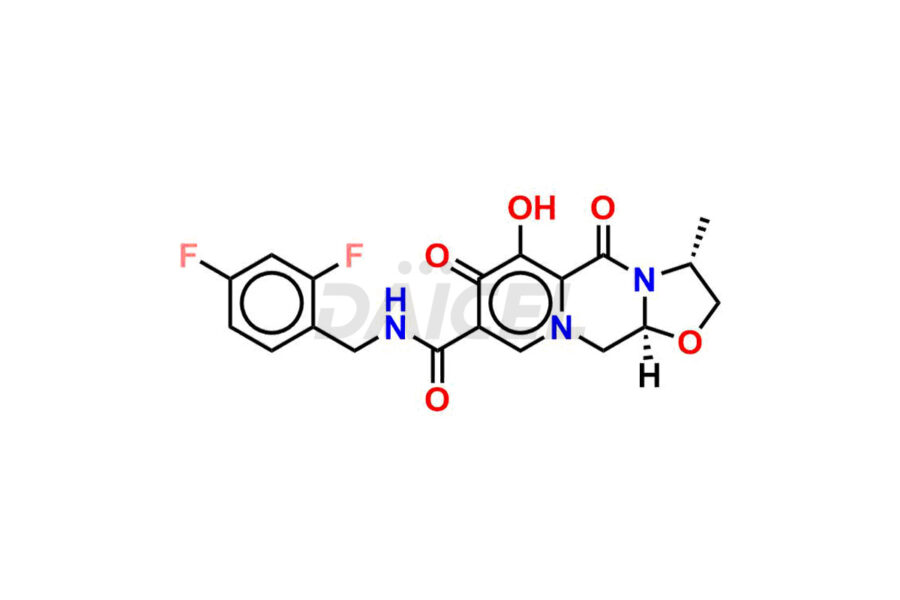
Ντάικελ Η Pharma συνθέτει ακαθαρσίες Cabotegravir εξαιρετικής ποιότητας, όπως Cabotegravir impurity 1, Cabotegravir Intermediate-1, Cabotegravir RR Isomer, Cabotegravir RS Isomer και Cabotegravir SS Isomer. Αυτές οι ακαθαρσίες είναι ζωτικής σημασίας για την αξιολόγηση της καθαρότητας, της αξιοπιστίας και της ασφάλειας του Cabotegravir, ενός δραστικού φαρμακευτικού συστατικού. Επιπλέον, η Daicel Pharma παρέχει προσαρμοσμένη σύνθεση ακαθαρσιών Cabotegravir για να καλύψει τις απαιτήσεις των πελατών για παράδοση σε όλο τον κόσμο.
Καβοτεγκραβίρη [CAS: 1051375-10-0], επίσης γνωστό ως GSK1265744A, είναι ένα φάρμακο για τη θεραπεία της λοίμωξης HIV-1. Είναι ένας αναστολέας ιντεγκράσης, που συχνά συνταγογραφείται παράλληλα με τον μη νουκλεοσιδικό αναστολέα της ανάστροφης μεταγραφάσης ριλπιβιρίνη. Η καβοτεγκραβίρη βοηθά στη θεραπεία της λοίμωξης HIV-1 σε άτομα που έχουν ιική καταστολή.
Cabotegravir: Χρήση και Εμπορική Διαθεσιμότητα
Το Cabotegravir είναι ένα συνταγογραφούμενο φάρμακο σε δύο μορφές και διατίθεται με δύο εμπορικές ονομασίες. Το Vocabria είναι ένα από του στόματος δισκίο σε συνδυασμό με ένα άλλο φάρμακο για τον HIV που ονομάζεται ριλπιβιρίνη (Edurant) για βραχυπρόθεσμη θεραπεία HIV-1 σε ενήλικες, ιολογικά κατασταλμένο. Το Apretude είναι μια ενέσιμη μορφή παρατεταμένης αποδέσμευσης Cabotegravir που θεραπεύει ενήλικες και εφήβους σε κίνδυνο που ζυγίζουν τουλάχιστον 35 Kg για προφύλαξη πριν από την έκθεση (PrEP) για τη μείωση του κινδύνου σεξουαλικά επίκτητης λοίμωξης HIV-1.
Δομή και Μηχανισμός Δράσης Cabotegravir 
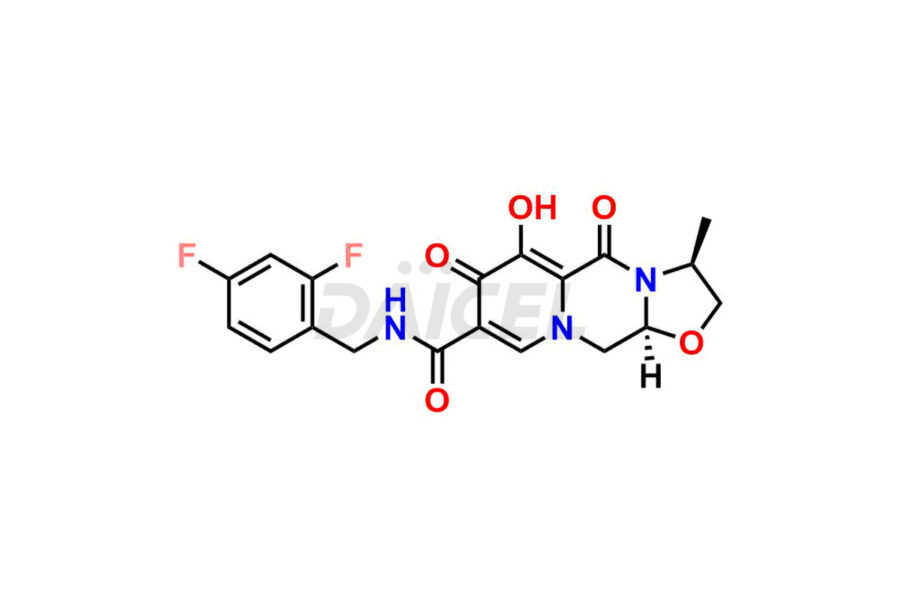
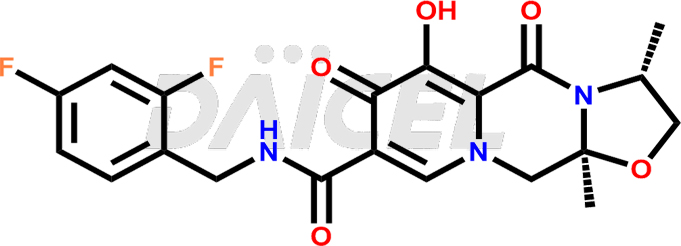
Η χημική ονομασία του Cabotegravir είναι (3S,11aR)-N-[(2,4-Διφθοροφαινυλ)μεθυλ]-2,3,5,7,11,11a-εξαϋδρο-6-υδροξυ-3-μεθυλ-5,7 -διοξοοξαζολο[3,2-a]πυριδο[1,2-d]πυραζινο-8-καρβοξαμίδιο. Ο χημικός του τύπος είναι C19H17F2N3O5και το μοριακό του βάρος είναι περίπου 405.4 g/mol.
Η καβοτεγκραβίρη δεσμεύεται στη δραστική θέση της HIV ιντεγκράσης και αναστέλλει την ιντεγκράση του HIV. Αναστέλλει το στάδιο μεταφοράς κλώνου της ενσωμάτωσης του ρετροϊικού δεοξυριβονουκλεϊκού οξέος (DNA) για τον κύκλο αντιγραφής του HIV.
Προσμείξεις καβοτεγκραβίρης και σύνθεση
Όπως κάθε άλλη φαρμακευτική ουσία, το Cabotegravir μπορεί να περιέχει ακαθαρσίες που επηρεάζουν την ασφάλεια και την αποτελεσματικότητά του. Αυτές οι ακαθαρσίες σχηματίζονται κατά τη διάρκεια της σύνθεσης1, καθαρισμός και αποθήκευση της φαρμακευτικής ουσίας. Μπορούν να περιλαμβάνουν ακαθαρσίες που σχετίζονται με τη διαδικασία, όπως υλικά έναρξης, αντιδραστήρια, ενδιάμεσα και προϊόντα αποικοδόμησης που προκύπτουν λόγω της χημικής ή φυσικής αστάθειας της φαρμακευτικής ουσίας ή της σύνθεσης της. Η παρουσία ακαθαρσιών μπορεί να δημιουργήσει δυνητικούς κινδύνους για τους ασθενείς, όπως τοξικότητα, μειωμένη δραστικότητα ή ανεπιθύμητες ενέργειες. Επομένως, είναι απαραίτητο να ελέγχετε και να παρακολουθείτε τα επίπεδα ακαθαρσιών στο Cabotegravir για να διασφαλιστεί ότι πληροί τα πρότυπα ποιότητας και ασφάλειας που απαιτούνται για τα φαρμακευτικά προϊόντα.
Η Daicel Pharma προσφέρει ένα Πιστοποιητικό Ανάλυσης (CoA) για πρότυπα ακαθαρσίας Cabotegravir, όπως Cabotegravir impurity 1, Cabotegravir Intermediate-1, Cabotegravir RR Isomer, Cabotegravir RS Isomer, και Cabotegravir SS Isomer, που δημιουργείται από ένα πρότυπο αναλυτής cMP για το FacGravir. Το CoA περιλαμβάνει μια ολοκληρωμένη αναφορά χαρακτηρισμού που περιλαμβάνει δεδομένα από τεχνικές όπως η καθαρότητα 1H NMR, 13C NMR, IR, MASS και HPLC2. Επιπλέον, κατόπιν αιτήματος, μπορούμε να παρέχουμε πρόσθετα δεδομένα όπως 13C-DEPT και CHN. Η Daicel Pharma μπορεί να συνθέσει άγνωστες προσμίξεις Cabotegravir ή προϊόντα αποδόμησης. Μια πλήρης αναφορά χαρακτηρισμού συνοδεύει κάθε παράδοση.
αναφορές
Συχνές Ερωτήσεις
αναφορές
- Johns, Brian Alvin; Kawasuji, Takashi; Taishi, Teruhiko; Taoda, Yoshiyuki, Bicyclic Carbamoylpyridone Derivative Having HIV Integrase Inhibiting Activity, Shionogi & Co., Ltd., Ιαπωνία, EP1852434B1, 13 Ιουλίου 2011
- Krishna Murthy Kasa, SR; Venkatanarayana, Muvvala; Chennuru, Lakshmi Narayana; Chandra Sekhara Rao, B.; Vemparala, Manohar; Chaman, Abdul Fareed; Ανάπτυξη μεθόδου Talluri, MVN Kumar, Chiral LC: Στερεοεκλεκτικός διαχωρισμός, χαρακτηρισμός και προσδιορισμός της καβοτεγκραβίρης και των σχετικών ισομερών ακαθαρσιών RS, RR και SS σε χειρόμορφη στατική φάση επικαλυμμένης με βάση την κυτταρίνη με HILIC-LC και LC-MS, Journal of Pharmaceutical and Biomedical Analysis, Τόμος: 222, Σελίδες: 115062, 2023
Συχνές Ερωτήσεις
Πώς ανιχνεύονται και αναλύονται οι ακαθαρσίες στο Cabotegravir;
Οι προσμείξεις στο Cabotegravir ανιχνεύονται και αναλύονται χρησιμοποιώντας αναλυτικές τεχνικές όπως η υγρή χρωματογραφία υψηλής απόδοσης (HPLC) και η υγρή χρωματογραφία-φασματομετρία μάζας (LC-MS). Αυτές οι τεχνικές βοηθούν στον εντοπισμό και τον ποσοτικό προσδιορισμό των ακαθαρσιών.
Πώς μπορούν οι ακαθαρσίες της Cabotegravir να επηρεάσουν τη σταθερότητα του φαρμακευτικού προϊόντος;
Οι προσμίξεις της καβοτεγκραβίρης μπορεί να επηρεάσουν τη σταθερότητα του φαρμακευτικού προϊόντος με αντίκτυπο στην ισχύ και την αποτελεσματικότητα του φαρμάκου. Ο έλεγχος των ακαθαρσιών είναι απαραίτητος για τη διασφάλιση της σταθερότητας και της διάρκειας ζωής του φαρμακευτικού προϊόντος.
Ποιος διαλύτης βοηθά στην ανάλυση των προσμείξεων Cabotegravir;
Το ακετονιτρίλιο ή η μεθανόλη είναι οι διαλύτες που χρησιμοποιούνται για την ανάλυση πολλών ακαθαρσιών στο Cabotegravir.
Ποιες είναι οι συνθήκες θερμοκρασίας που απαιτούνται για την αποθήκευση των ακαθαρσιών της Cabotegravir;
Οι προσμείξεις της καβοτεγκραβίρης αποθηκεύονται σε ελεγχόμενη θερμοκρασία δωματίου μεταξύ 2-8 °C ή όπως υποδεικνύεται στο Πιστοποιητικό Ανάλυσης (CoA).
Σημείωση: Τα προϊόντα που προστατεύονται από έγκυρα διπλώματα ευρεσιτεχνίας από έναν κατασκευαστή δεν προσφέρονται προς πώληση σε χώρες που διαθέτουν προστασία ευρεσιτεχνίας. Η πώληση τέτοιων προϊόντων συνιστά παραβίαση διπλώματος ευρεσιτεχνίας και η ευθύνη της είναι με ευθύνη του αγοραστή.