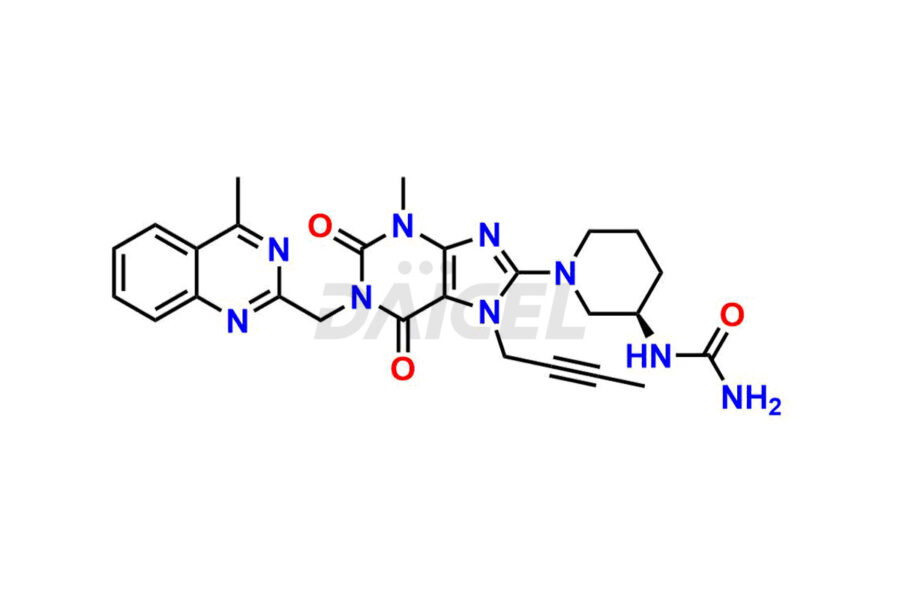
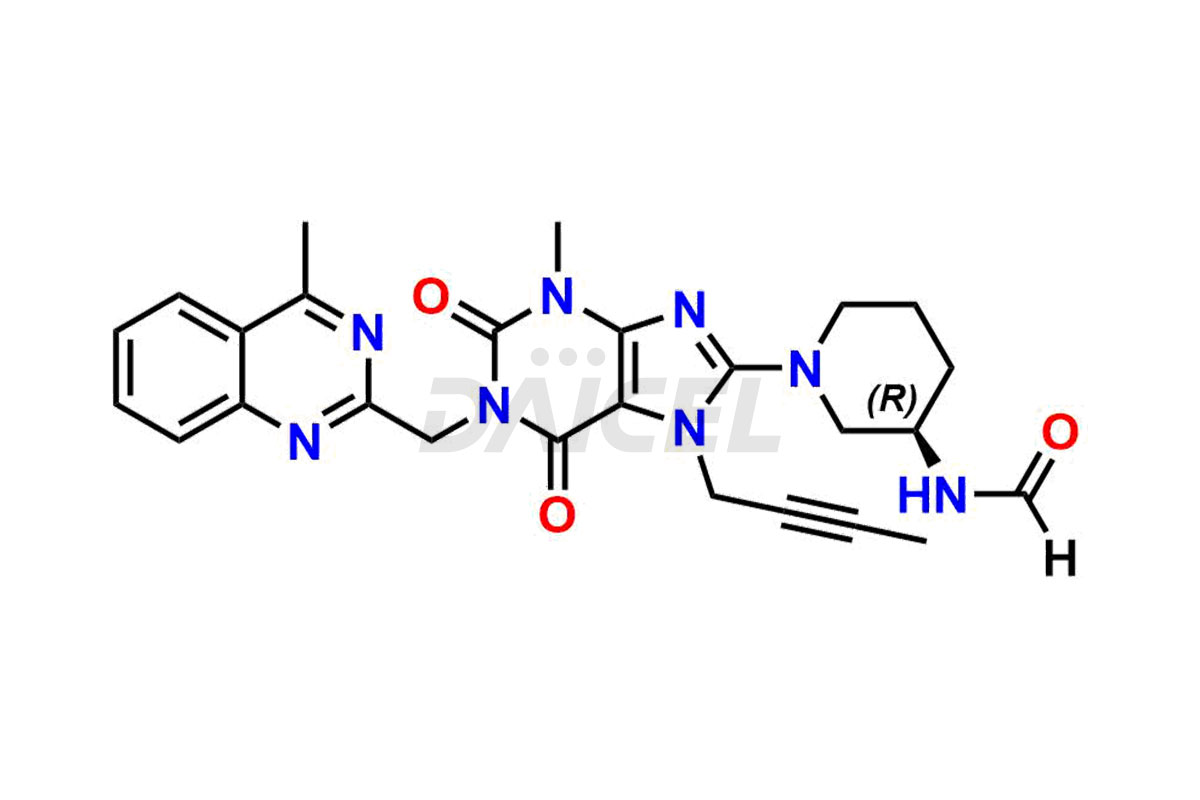
Linagliptin
Bibliographie
- Himmelsbach, Frank; Langkopf, Elke; Eckhardt, Matthias; Mark, Michael; Maier, Roland; Lotz, Ralf Richard Hermann; Tadayyon, Mohammad, 8-[3-amino-piperidin-1-yl]-xanthine, deren Herstellung und ihre Verwendung als pharmazeutische Zusammensetzungen, Boehringer Ingelheim Pharma GmbH & Co. K.-G., Deutschland, US7407955B2, 5. August, 2008
- El-Bagary, Ramzia Ismail; Elkady, Ehab Farouk; Ayoub, Bassam Mahfouz, Spektrofluorometrische Bestimmung von Linagliptin in loser Schüttung und in pharmazeutischer Dosierungsform, European Journal of Chemistry, Band: 5, Ausgabe: 2, Seiten: 380-382, 3 Seiten, 2014
Häufig gestellte Fragen
Gibt es spezielle Richtlinien oder Anforderungen für die Meldung von Linagliptin-Verunreinigungen?
Regulatorische Richtlinien beschreiben die notwendige Dokumentation und Meldung von Linagliptin-Verunreinigungen, um Transparenz und Rechenschaftspflicht zu gewährleisten.
Werden Linagliptin-Verunreinigungen auf ihr genotoxisches Potenzial getestet?
Genotoxizitätstests werden typischerweise durchgeführt, um das Potenzial von Linagliptin-Verunreinigungen zu beurteilen, DNA-Schäden oder Mutationen zu verursachen.
Können Verunreinigungen von Linagliptin auf unzureichende Herstellungsprozesse zurückzuführen sein?
Unsachgemäße Herstellungsprozesse, wie etwa unsachgemäße Handhabung oder Kontamination, können zur Bildung von Verunreinigungen in Linagliptin beitragen.
Was ist die empfohlene Lagertemperatur für Linagliptin-Verunreinigungen?
Linagliptin-Verunreinigungen sollten bei kontrollierter Raumtemperatur, normalerweise zwischen 2 und 8 °C, gelagert werden.
Hinweis: Produkte, die durch gültige Patente eines Herstellers geschützt sind, werden in Ländern mit Patentschutz nicht zum Verkauf angeboten. Der Verkauf solcher Produkte stellt eine Patentverletzung dar und die Haftung erfolgt auf Risiko des Käufers.