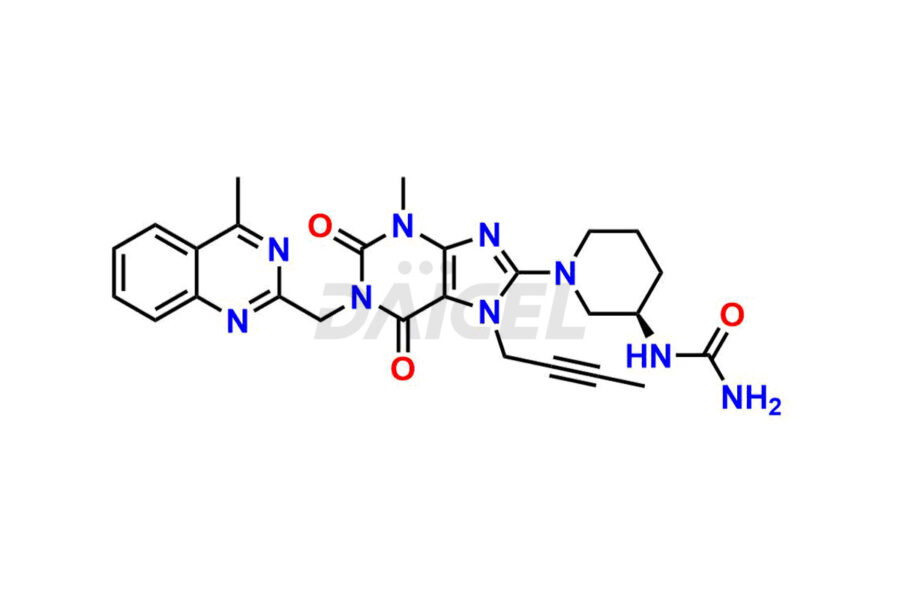
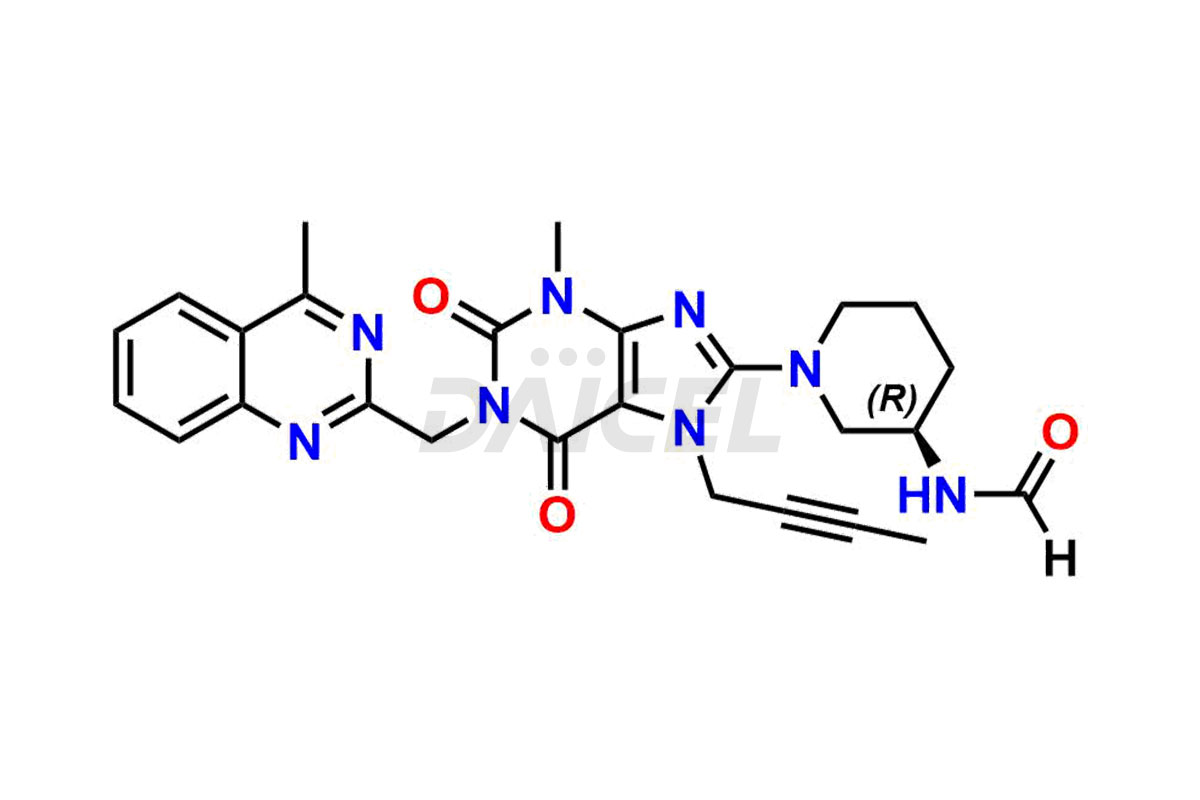
Linagliptyna
Referencje
- Himmelsbach, Frank; Langkopf, Elke; Eckhardt, Matthias; Marek, Michał; Maiera, Rolanda; Lotz, Ralf Richard Hermann; Tadayyon, Mohammad, 8-[3-amino-piperydyn-1-ylo]-ksantyny, ich wytwarzanie i ich zastosowanie jako kompozycje farmaceutyczne, Boehringer Ingelheim Pharma GmbH & Co. K.-G., Niemcy, US7407955B2, 5 sierpnia, 2008
- El-Bagary, Ramzia Ismail; Elkady, Ehab Farouk; Ayoub, Bassam Mahfouz, Spektrofluorometryczne oznaczanie linagliptyny w masie i w farmaceutycznej formie dawki, European Journal of Chemistry, tom: 5, wydanie: 2, strony: 380-382, 3 s., 2014
Często Zadawane Pytania
Czy istnieją jakieś szczególne wytyczne lub wymagania dotyczące zgłaszania zanieczyszczeń linagliptyną?
Wytyczne regulacyjne określają niezbędną dokumentację i zgłaszanie zanieczyszczeń linagliptyną, aby zapewnić przejrzystość i rozliczalność.
Czy zanieczyszczenia linagliptyną są badane pod kątem ich potencjału genotoksycznego?
Badanie genotoksyczności zazwyczaj przeprowadza się w celu oceny potencjału zanieczyszczeń linagliptyną, które mogą powodować uszkodzenia lub mutacje DNA.
Czy zanieczyszczenia linagliptyną mogą wynikać z nieodpowiednich procesów produkcyjnych?
Niewłaściwe procesy produkcyjne, takie jak niewłaściwe obchodzenie się z lekiem lub zanieczyszczenie, mogą przyczynić się do powstawania zanieczyszczeń w linagliptynie.
Jaka jest zalecana temperatura przechowywania zanieczyszczeń Linagliptyną?
Zanieczyszczenia linagliptyną należy przechowywać w kontrolowanej temperaturze pokojowej, zwykle pomiędzy 2–8°C.
Uwaga: Produkty chronione ważnymi patentami przez producenta nie są oferowane do sprzedaży w krajach posiadających ochronę patentową. Sprzedaż takich produktów stanowi naruszenie patentu, a jej odpowiedzialność ponosi kupujący.