Informacje ogólne
Bortezomib Zanieczyszczenia i Bortezomib
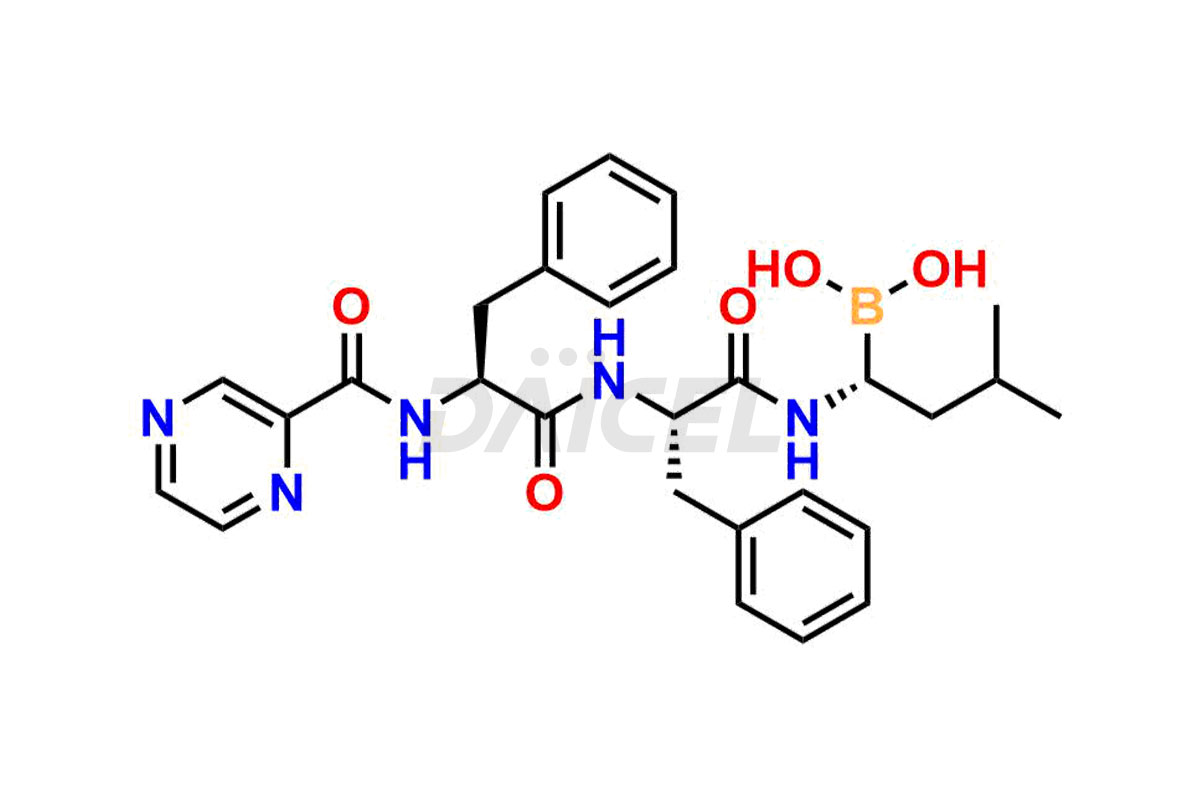
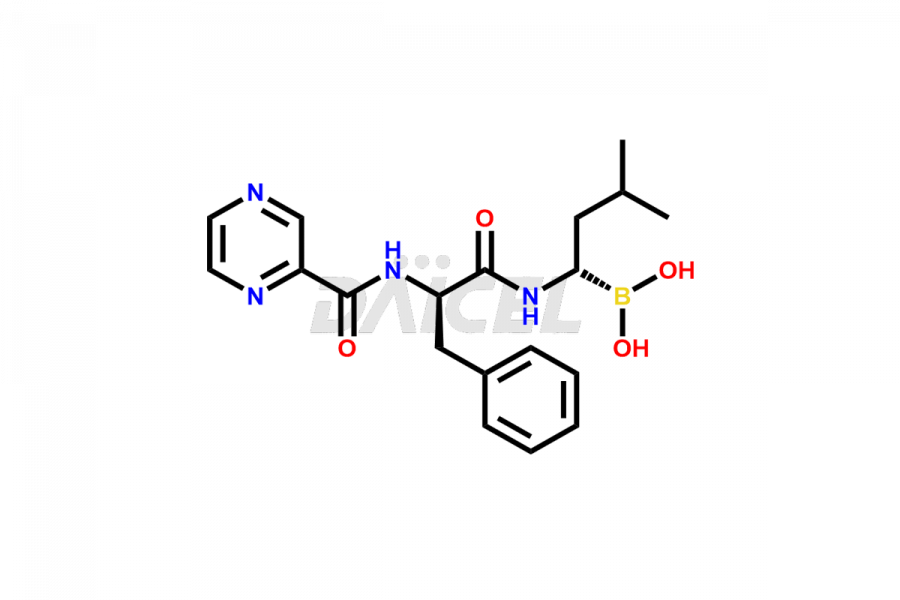
Daicel Pharma syntetyzuje wysokiej jakości zanieczyszczenia bortezomibem, w tym zanieczyszczenie kwasem bortezomibu, zanieczyszczenie amidem bortezomibu, dimer bortezomibu i enancjomer bortezomibu. Te zanieczyszczenia są niezbędne do oceny jakości, stabilności i bezpieczeństwa aktywnego składnika farmaceutycznego, bortezomibu. Ponadto Daicel Pharma oferuje zindywidualizowaną syntezę zanieczyszczeń Bortezomibu z dostawą na całym świecie, aby spełnić specyficzne potrzeby naszych klientów.
Bortezomib [KAS: 179324-69-7] jest lekiem przeciwnowotworowym i inhibitorem proteasomu, który leczy chłoniaki i opornego na leczenie szpiczaka mnogiego. Jest to zmodyfikowana pochodna kwasu dipeptydyloboronowego stosowana w leczeniu szpiczaka mnogiego.
Bortezomib: zastosowanie i dostępność komercyjna
Bortezomib jest zatwierdzonym przez FDA lekiem przeciwnowotworowym do leczenia szpiczaka mnogiego. Leczy również chłoniaka z komórek płaszcza u pacjentów poddanych co najmniej jednemu wcześniejszemu leczeniu pierwszego rzutu. Velcade to marka, pod którą dostępny jest Bortezomib.
Struktura bortezomibu i mechanizm działania
Nazwa chemiczna bortezomibu to kwas [(1R)-3-metylo-1-[[(2S)-1-okso-3-fenylo-2-[(pirazynylokarbonylo)amino]propylo]amino]butylo]-borowy. Jego wzór chemiczny to C19H25BN4O4, a jego masa cząsteczkowa wynosi około 384.2 g/mol.
Bortezomib hamuje proteasom 26S w komórkach ssaków, co zapobiega proteolizie. Zaburza homeostatyczne mechanizmy prowadzące do śmierci komórki i opóźnia wzrost guza.
Zanieczyszczenia i synteza bortezomibu
Zanieczyszczenia powstające podczas produkcji1 procesu lub przechowywania bortezomibu obejmują produkty degradacji i zanieczyszczenia związane z procesem, pozostałości rozpuszczalników i pozostałości metali. Mogą one wpływać na bezpieczeństwo, skuteczność i jakość leków. Konieczna jest więc ich kontrola poprzez stosowanie odpowiednich środków, takich jak stosowanie wysokiej jakości materiałów wyjściowych, optymalizacja procesu wytwarzania, stosowanie odpowiednich warunków przechowywania oraz przeprowadzanie rygorystycznych badań kontroli jakości, aby zapewnić czystość i bezpieczeństwo produktu leczniczego.
Daicel Pharma zapewnia certyfikat analizy (CoA) dla standardów zanieczyszczeń bortezomibem, w tym zanieczyszczenia kwasem bortezomibu, zanieczyszczenia amidem bortezomibu, dimeru bortezomibu i enancjomeru bortezomibu. CoA jest generowane z urządzenia analitycznego zgodnego z cGMP i zawiera obszerne dane charakteryzujące, takie jak czystość 1H NMR, 13C NMR, IR, MASS i HPLC2. Na życzenie możemy również podać dodatkowe dane charakterystyczne, takie jak 13C-DEPT i CHN. Daicel Pharma może tworzyć nieznane zanieczyszczenia Bortezomibem lub produkty degradacji. Każda dostawa posiada pełny raport z charakterystyki.