Etyl 3-amino-2-(((2′-cyjano-[1,1′-bif...
- NUMER KOTA DCTI-C-3254
- NUMER CAS 136285-69-3
- FORMUŁA MOLEKULARNA C23H21N3O2
- WAGA MOLEKULARNA 371.44
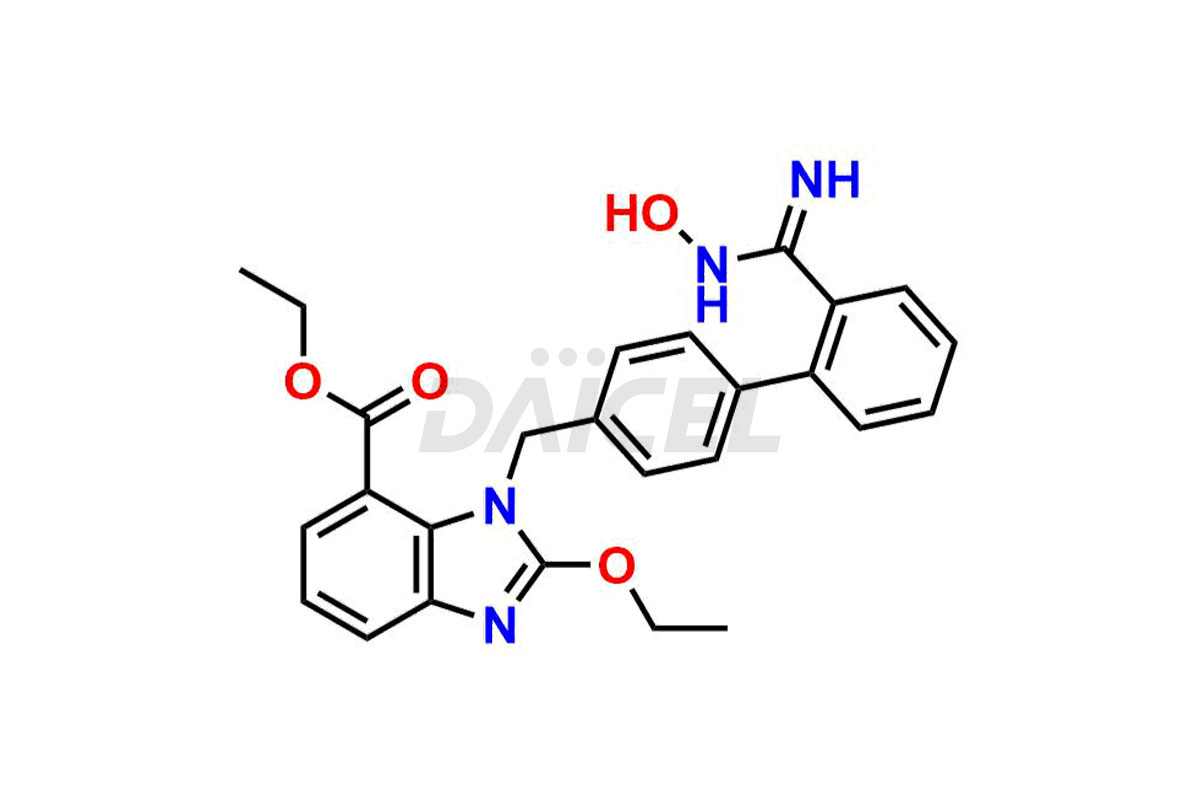
Etylo-2-etoksy-3-((2′-(N'-hydroksykarbaMimidoil)
- Numer KAT DCTI-C-1336
- Numer CAS 1397836-41-7
- Molecular Formula C26H26N4O4
- Waga molekularna 458.52
ZAŁADUJ WIĘCEJ
Oglądasz wszystkie 11 produktów