abakawir
Informacje ogólne
Abakawir Zanieczyszczenia i Abakawir
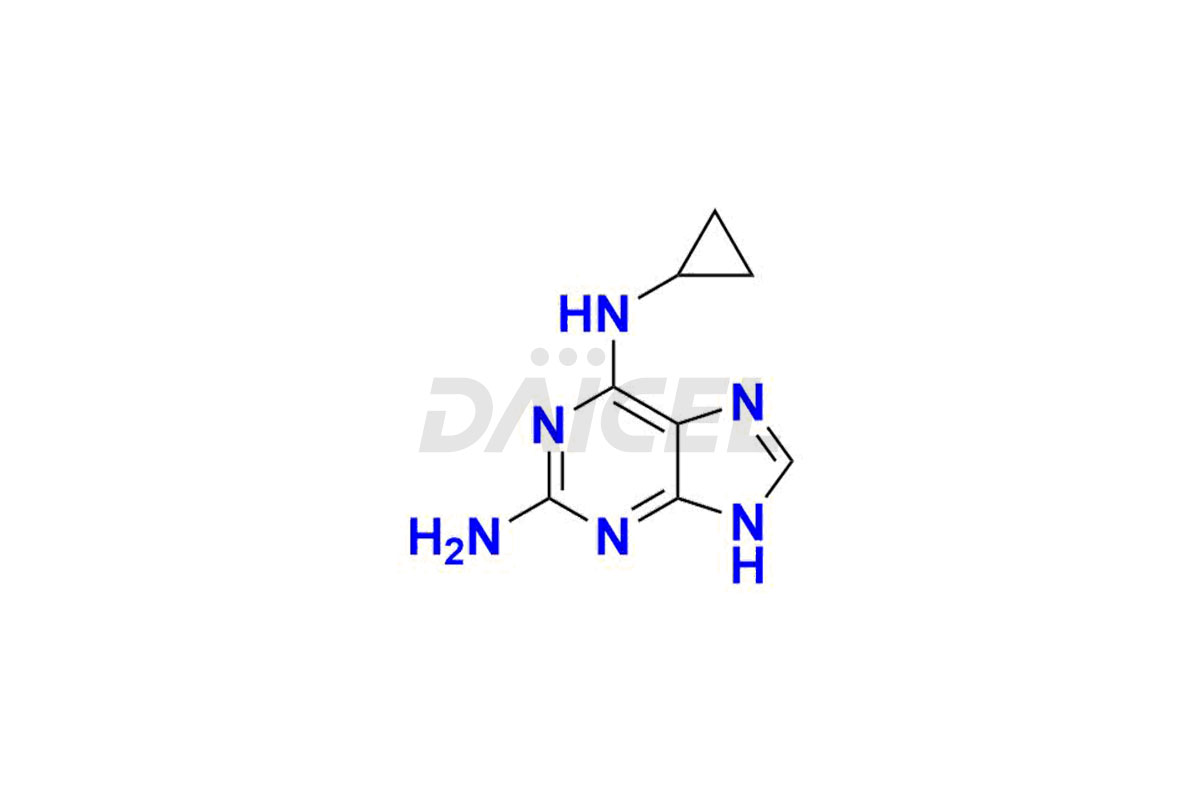
Firma Daicel Pharma syntetyzuje wysokiej jakości zanieczyszczenie abakawirem, N6-cyklopropylo-9H-puryno-2,6-diaminę, co ma kluczowe znaczenie w analizie jakości, stabilności i bezpieczeństwa biologicznego aktywnego składnika farmaceutycznego Abakawiru. Ponadto Daicel Pharma oferuje niestandardową syntezę zanieczyszczeń Abacavir i dostarcza je na całym świecie.
abakawir [KAS: 136470-78-5] jest syntetycznym karbocyklicznym analogiem nukleozydu stosowanym w leczeniu zakażenia wirusem HIV u dorosłych, dzieci i niemowląt. Łączy się z innymi lekami na HIV, zwłaszcza siarczanami i innymi lekami przeciwretrowirusowymi. Abakawir działa jako nukleozydowy analogowy inhibitor odwrotnej transkryptazy (NRTI), który pomaga zwalczać HIV poprzez hamowanie aktywności enzymu odwrotnej transkryptazy HIV-1, który jest niezbędny do replikacji wirusa.
Abakawir: zastosowanie i dostępność komercyjna
Abakawir jest zatwierdzonym przez FDA lekiem do leczenia zakażenia wirusem HIV-1. Jest stosowany w połączeniu z innymi lekami przeciwretrowirusowymi, takimi jak abakawir/lamiwudyna/zydowudyna, abakawir/dolutegrawir/lamiwudyna i abakawir/lamiwudyna. Abakawir jest sklasyfikowany jako nukleozydowy inhibitor odwrotnej transkryptazy (NRTI) i może być podawany doustnie w postaci tabletki lub roztworu. Nazwy handlowe abakawiru obejmują Epzicom (połączenie abakawiru-lamiwudyny), Triumeq (połączenie abakawiru-lamiwudyny-dolutegrawiru), Trizivir (połączenie abakawiru-lamiwudyny-zydowudyny) i Ziagen.
Struktura abakawiru i mechanizm działania 
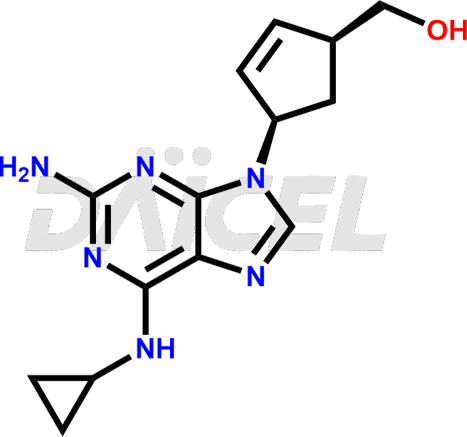
Nazwa chemiczna abakawiru to (1S,4R)-4-[2-amino-6-(cyklopropylamino)-9H-puryn-9-ylo]-2-cyklopenteno-1-metanol. Jego wzór chemiczny to C14H18N6O, a jego masa cząsteczkowa wynosi około 286.33 g/mol.
Abakawir jest przekształcany do swojego aktywnego metabolitu, trójfosforanu karbowiru. Jest analogiem deoksyguanozyno-5¢-trifosforanu (dGTP). Hamuje aktywność odwrotnej transkryptazy (RT) wirusa HIV-1.
Zanieczyszczenia i synteza abakawiru
Zanieczyszczenia abakawirem można podzielić na kategorie według materiałów wyjściowych, procesu reakcji lub degradacji substancji leczniczej. Powstałe zanieczyszczenia mogą wynikać z procesu syntezy1, etapy oczyszczania lub warunki przechowywania. Mogą wpływać na jakość, bezpieczeństwo i skuteczność leku. Regularne monitorowanie i analiza pomagają zapewnić, że poziomy zanieczyszczeń pozostają w dopuszczalnych granicach i nie stanowią zagrożenia dla pacjentów.
Daicel dostarcza Certyfikat Analizy (CoA) dla standardu zanieczyszczeń abakawiru, N6-cyklopropylo-9H-puryno-2,6-diaminy. Certyfikat CoA jest wydawany przez placówkę analityczną zgodną z cGMP i zawiera pełne dane dotyczące charakterystyki, takie jak czystość 1H NMR, 13C NMR, IR, MASS i HPLC2. Dodatkowe dane charakterystyczne, takie jak 13C-DEPT i CHN, mogą być dostarczone na żądanie. Daicel może również przygotować dowolne nieznane zanieczyszczenie lub produkt degradacji abakawiru. Dajemy pełny raport z charakterystyki przy dostawie.
Referencje
- Daluge, Susan Mary, Therapeutic nucleosides, Wellcome Foundation Ltd., Wielka Brytania, US5034394A, 23 lipca 1991
- Veldkamp, AI; Sparidans, RW; Hoetelmans, RMW; Beijnen, JH, Ilościowe oznaczanie abakawiru (1592U89), nowego nukleozydowego inhibitora odwrotnej transkryptazy, w ludzkim osoczu za pomocą izokratycznej wysokosprawnej chromatografii cieczowej z odwróconymi fazami z wykrywaniem ultrafioletu, Journal of Chromatography B: Biomedical Sciences and Applications, tom: 736, Wydanie: 1 + 2, Strony: 123-128, 1999
Często Zadawane Pytania
Jakie jest źródło zanieczyszczeń Abakawirem?
Źródłem zanieczyszczeń abakawirem mogą być surowce, rozpuszczalniki, odczynniki i produkty degradacji powstające podczas wytwarzania lub przechowywania produktu leczniczego.
W jaki sposób wykrywa się i określa ilościowo zanieczyszczenia w Abakavir?
Abakawir Zanieczyszczenia są wykrywane i oznaczane ilościowo za pomocą technik chromatograficznych i spektroskopowych, takich jak HPLC, UPLC i LC-MS.
W jaki sposób monitoruje się zanieczyszczenia abakawirem?
Zanieczyszczenia abakawiru są monitorowane poprzez regularne badania substancji leczniczej i produktu podczas produkcji i przez cały okres jego przydatności do spożycia.
W jakich warunkach temperaturowych należy przechowywać zanieczyszczenia abakawirem?
Zanieczyszczenia abakawirem są przechowywane w kontrolowanej temperaturze pokojowej w zakresie 2–8 ⁰C lub zgodnie ze wskazaniami w certyfikacie analizy (CoA).
Uwaga: Produkty chronione ważnymi patentami przez producenta nie są oferowane do sprzedaży w krajach posiadających ochronę patentową. Sprzedaż takich produktów stanowi naruszenie patentu, a jej odpowiedzialność ponosi kupujący.