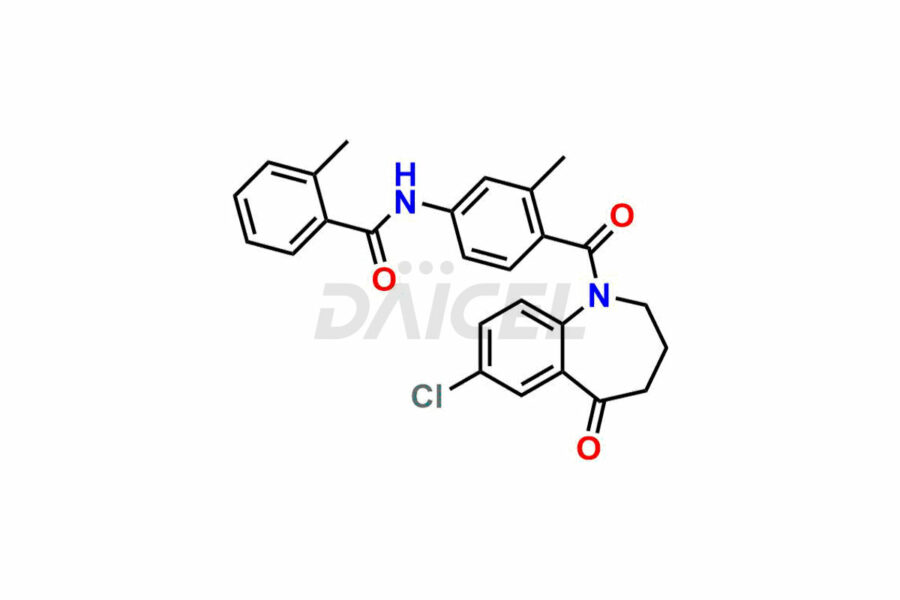
Tolvaptán
Referencias
- Ogawa, Hidenori; Miyamoto, Hisashi; Kondo, Kazumi; Yamashita, Hiroshi; Nakaya, Kenji; Komatsu, Hajime; Tanaka, Michinori; Takara, Shinya; Tominaga, Michiaki; Yabuchi, Yoichi, Compuestos benzoheterocíclicos, Otsuka Pharmaceutical Co., Ltd., Japón, US5258510A, 2 de noviembre de 1993
- Pei, Qi; Zhang, Bikui; Bronceado, Hongyi; Liu, Lihua; Peng, Xiangdong; Li, Zuojun; Huang, Panhao; Luo, Mi; Zuo, Xiaocong; Guo, Chengxian; et al, Desarrollo y validación de un método LC-MS/MS para la determinación de tolvaptán en plasma humano y su aplicación a un estudio farmacocinético, Journal of Chromatography B: Analytical Technologies in the Biomedical and Life Sciences, Volumen: 913-914, Páginas: 84-89, 2013
Preguntas frecuentes
¿Se emplean técnicas analíticas particulares para garantizar el control de impurezas en el tolvaptán?
Muchos métodos analíticos validados, como la cromatografía líquida de alto rendimiento en fase inversa (RP-HPLC) junto con un método UV, ayudan a detectar y cuantificar las impurezas en el tolvaptán.
¿Qué medidas ayudan a minimizar las impurezas de tolvaptán durante el almacenamiento del medicamento?
Las condiciones de almacenamiento adecuadas, como el control de la temperatura y la protección contra la luz y la humedad, ayudan a minimizar la formación de impurezas.
¿Qué disolvente ayuda en el análisis de impurezas de tolvaptán?
El metanol ayuda a analizar muchas impurezas del tolvaptán.
¿Cuáles son las condiciones de temperatura necesarias para almacenar las impurezas de tolvaptán?
Las impurezas de tolvaptán se almacenan a temperatura ambiente controlada entre 2 y 8 °C o como se indica en el Certificado de análisis (CoA).
Nota: Los productos protegidos por patentes válidas de un fabricante no se ofrecen a la venta en países que cuentan con protección de patentes. La venta de tales productos constituye una infracción de patente, y su responsabilidad es por cuenta y riesgo del comprador.