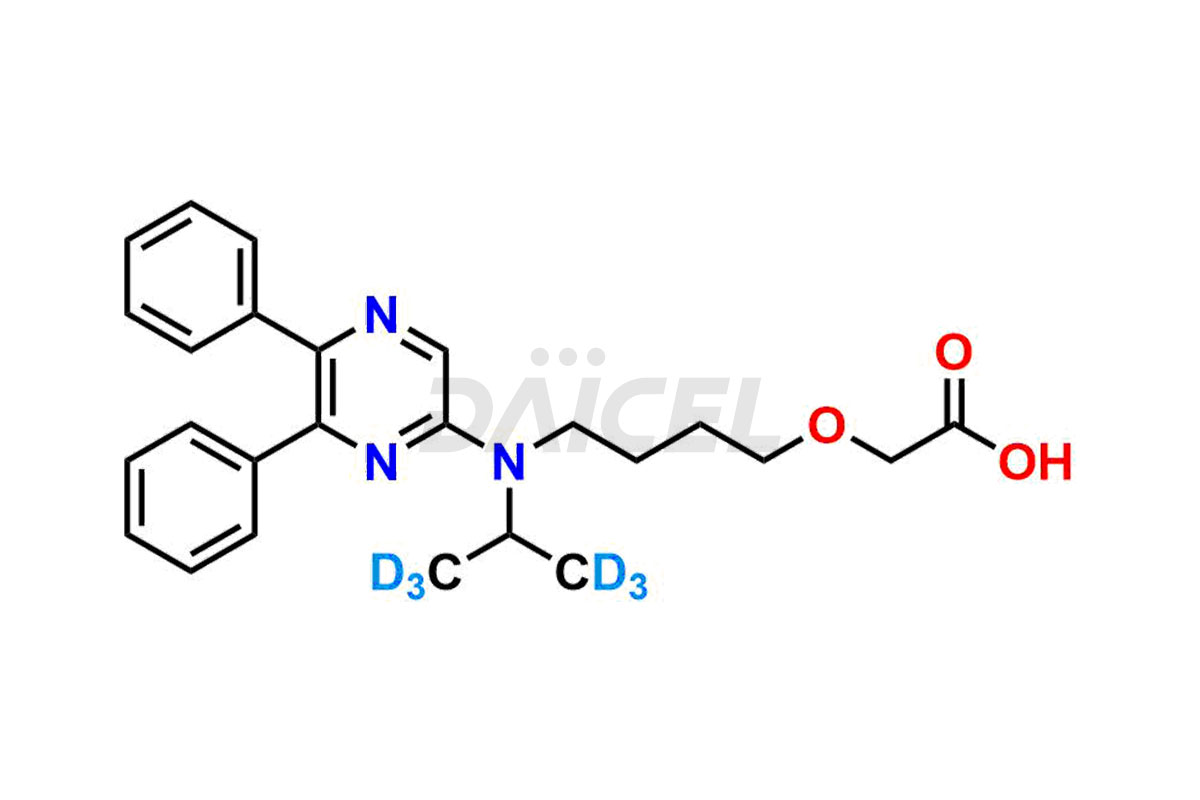
Selexipag
Referencias
- Asaki, Tetsuo; Hamamoto, Taisuke; Kuwano, Keiichi, Derivados de compuestos heterocíclicos y medicamentos, Nippon Shinyaku Co., Ltd., Japón, EP1400518B1, 17 de enero de 2007
- Bonde, Prajakta G.; Bachhav, RS; Kalegaonkar, Somnath, Desarrollo y validación del método RP-HPLC para la estimación de selexipag a granel y su forma de dosificación en comprimidos, World Journal of Pharmacy and Pharmaceutical Sciences, volumen: 11, número: 8, páginas: 2166-2175, 2022
Preguntas frecuentes
¿Por qué la presencia de impurezas es una preocupación en Selexipag?
La presencia de impurezas en Selexipag puede afectar significativamente su calidad, seguridad y eficacia. Según el tipo y la concentración de las impurezas, pueden afectar negativamente a la actividad farmacológica y la estabilidad del fármaco y, en última instancia, plantear riesgos potenciales para la salud del paciente. Por lo tanto, es fundamental gestionar y controlar cuidadosamente las impurezas para garantizar el rendimiento y la seguridad óptimos del fármaco como producto farmacéutico.
¿Cómo se detectan y cuantifican las impurezas en Selexipag?
Las impurezas de Selexipag se evalúan mediante técnicas analíticas como el novedoso método de cromatografía líquida de alta resolución (RP-HPLC).
¿Qué disolventes ayudan en el análisis de las impurezas de Selexipag?
El metanol es el disolvente utilizado en las técnicas analíticas para separar y detectar las impurezas de Selexipag.
¿Cuáles son las condiciones de temperatura requeridas para almacenar las impurezas de Selexipag?
Las impurezas de Selexipag deben almacenarse a una temperatura ambiente controlada entre 2 y 8 °C o según lo indicado en el Certificado de análisis (CoA).
Nota: Los productos protegidos por patentes válidas de un fabricante no se ofrecen a la venta en países que cuentan con protección de patentes. La venta de tales productos constituye una infracción de patente, y su responsabilidad es por cuenta y riesgo del comprador.