Cefalotina lactona
- Número de CAT DCTI-C-1468
- CAS 10590-10-0
- Fórmula molecular C14H12N2O4S2
- Peso molecular 336.38 (base libre)
Impureza de metoxicefalotina
- Número de CAT DCTI-C-1696
- CAS 35565-06-1
- Fórmula molecular C17H18N2O7S2
- Peso molecular 426.46
Farmacia Daicel sintetiza impurezas de cefalotina de alta calidad, cefalotina lactona e impurezas de metoxicefalotina, que son cruciales en el análisis de la calidad, la estabilidad y la seguridad biológica del ingrediente farmacéutico activo, la cefalotina. Además, Daicel Pharma ofrece síntesis personalizada de impurezas de cefalotina y las entrega a nivel mundial.
Cefalotina [CAS: 153-61-7] es un fármaco antibacteriano que pertenece a la clase de antibióticos de cefalosporina de primera generación. Es un antibiótico betalactámico semisintético que mata las bacterias. Se usa por vía parenteral durante la cirugía y para tratar infecciones de la sangre. Además, la cefalotina es un agente antimicrobiano.
La cefalotina trata infecciones bacterianas que afectan el tracto urinario, el tracto respiratorio inferior, tejidos blandos, huesos y articulaciones, infecciones de la piel, peritonitis, sepsis, osteomielitis, mastitis, infecciones posoperatorias y heridas infectadas. Está disponible en todo el mundo bajo marcas como Arecamin, Baccef, Cefadin, Ceftina, Ceporacin, Cepovenin, Falot, Jnflin y Practogen, etc.
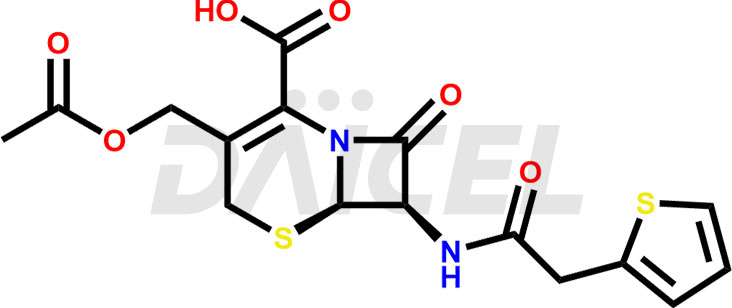
El nombre químico de la cefalotina es 3-(acetoximetil)-8-oxo-7-[2-(2-tienil)acetamido]-5-tia-1-azabiciclo[4.2.0]oct-2-eno-2-carboxílico ácido. Su fórmula química es C16H16N2O6S2, y su peso molecular es de aproximadamente 396.4 g/mol.
La cefalotina se une a las proteínas de unión a penicilina (PBP) ubicadas en la membrana interna de las células bacterianas. La inactivación de las PBP provoca un debilitamiento de la pared celular bacteriana y, finalmente, la lisis de la célula bacteriana.
Durante la fabricación1 proceso de cefalotina, impurezas2 pueden formarse en el fármaco que presentan riesgos potenciales para la salud de los pacientes. Estas impurezas pueden formarse debido a la degradación o subproductos de los intermedios de reacción, incluidas las impurezas epiméricas y los productos de degradación. Es vital monitorear los niveles de impurezas en la medicación para garantizar su seguridad y eficacia en el tratamiento de los pacientes.
Daicel ofrece un Certificado de análisis (CoA) de una instalación analítica que cumple con las cGMP para los estándares de impureza de cefalotina, lactona de cefalotina y la impureza de cefalotina metoxi. El CoA incluye datos completos de caracterización, como 1H NMR, 13C NMR, IR, MASS y pureza HPLC. También proporcionamos 13C-DEPT y CHN a pedido. Damos un completo informe de caracterización en el momento de la entrega.
Daicel tiene la tecnología y la experiencia para preparar cualquier producto de degradación o impureza de cefalotina desconocido. También proporcionamos compuestos etiquetados para cuantificar la eficacia de la cefalotina genérica. Daicel ofrece estándares de cefalotina marcados con isótopos de alta pureza para investigación bioanalítica y estudios BA/BE con datos de isótopos en CoA.
La síntesis de impurezas de cefalotina se realiza a través de diversas reacciones químicas, como hidrólisis, oxidación y desaminación de cefalotina y sus intermediarios.
Los métodos analíticos como la cromatografía líquida de alta resolución (HPLC) ayudan a identificar y cuantificar la cefalotina.
La síntesis de impurezas de cefalotina es un desafío debido a la complejidad de las reacciones químicas involucradas y la necesidad de experiencia y equipo especializado.
Los métodos alternativos para sintetizar impurezas de cefalotina incluyen el uso de enzimas microbianas y biocatálisis.
Nota: Los productos protegidos por patentes válidas de un fabricante no se ofrecen a la venta en países que cuentan con protección de patentes. La venta de tales productos constituye una infracción de patente, y su responsabilidad es por cuenta y riesgo del comprador.