Importancia de los péptidos cíclicos y papel de las impurezas
Fármacos peptídicos cíclicos y su importancia
Los péptidos cíclicos son una clase de moléculas que han atraído una atención significativa en el desarrollo de fármacos debido a sus propiedades únicas, que incluyen alta estabilidad, especificidad de objetivo, potencia mejorada y permeabilidad celular. Los péptidos cíclicos son cadenas polipeptídicas que tienen una estructura de anillo cíclico que consta de 5 a 14 aminoácidos con un peso molecular de aproximadamente 500 a 2000 Da. La estructura de anillo se puede formar uniendo un extremo del péptido y el otro con un enlace amida u otros enlaces químicamente estables como lactona, éter, tioéter, disulfuro, etc.
La ciclación de secuencias de péptidos ayuda a unirse de manera más eficiente con sus respectivos receptores. La estructura cíclica de los péptidos proporciona una gran superficie para la interacción con el sitio objetivo. Los fármacos de péptidos cíclicos son impermeables a la hidrólisis enzimática ya que no tienen extremos amino y carboxilo libres, lo que mejora su estabilidad. Por lo general, los péptidos cíclicos muestran una mejor actividad biológica en comparación con sus contrapartes lineales debido a la estructura conformacional, lo que permite una unión mejorada hacia las moléculas objetivo o la selectividad por parte del receptor.
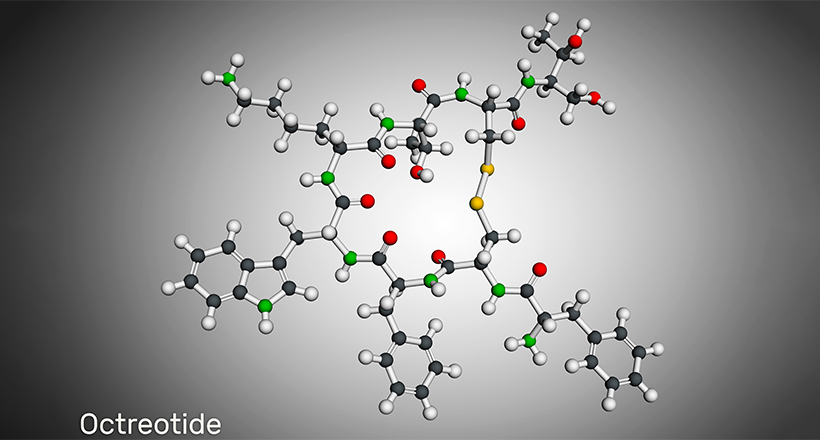
Algunos medicamentos de péptidos cíclicos incluyen Daptomicina, Telavancina, Dalbavancina, Lanreotida, Octreotida, Linaclotida, Plecanatida, Romidepsina, vasopresina, La oxitocinay Calcitonina. Muchos medicamentos de péptidos cíclicos provienen de fuentes naturales como la ciclosporina A, la bactenecina, la lactociclina y más. Sin embargo, los medicamentos de péptidos cíclicos sintéticos creados con bioingeniería se están volviendo comunes ahora.
¿Cómo se sintetizan los péptidos cíclicos?
La síntesis de péptidos cíclicos implica la síntesis de péptidos en fase sólida (SPPS). En este método, la síntesis de péptidos se produce de forma lineal, inmovilizados en una perla de resina con un conector disulfuro u otros enlaces químicamente estables, como lactona, éter y tioéter. Después de la formación del péptido lineal, los posibles grupos protectores se escinden y los péptidos se liberan al agregar una base. Además, la desprotonación del grupo tiol N-terminal golpea el conector disulfuro entre el péptido y la resina en la ciclación intramolecular, dando el péptido cíclico deseado.
En general, la síntesis de péptidos cíclicos requiere un control cuidadoso de los grupos protectores, los reactivos de acoplamiento y las condiciones de reacción para garantizar altos rendimientos y pureza.
Técnicas de Síntesis de Péptidos Cíclicos
La preparación de compuestos peptídicos cíclicos utiliza varias técnicas: • química combinatoria • síntesis de novo. • ciclación mediada por ligadura quimioselectiva
Dependiendo de la ciclación, los métodos para sintetizar péptidos cíclicos son de cabeza a cola, de cadena lateral a cadena lateral, de cabeza a cadena lateral y de cadena lateral a cola. La ciclación de los aminoácidos de la cadena lateral se produce con la formación de puentes disulfuro entre las cisteínas. Además, la ciclación de esqueleto a esqueleto se realiza mediante la formación de enlaces amida entre los residuos de aminoácidos N-terminal y C-terminal.
Además, existen otros péptidos cíclicos como los péptidos bicíclicos/tricíclicos y los péptidos cíclicos grapados. Los péptidos bicíclicos son inhibidores enzimáticos efectivos y los péptidos grapados facilitan la penetración de las células peptídicas y utilizan agentes de entrecruzamiento para mejorar las propiedades fisicoquímicas.
Impurezas en fármacos de péptidos cíclicos
Las impurezas pueden surgir de la síntesis de péptidos cíclicos. Las impurezas relacionadas con API son truncamientos, modificaciones de grupos funcionales, inserción o eliminación de aminoácidos, oxidaciones o reducción de grupos funcionales, agregados y desprotección incompleta. Los medios cromatográficos utilizados en la purificación y los disolventes también pueden contribuir a la generación de impurezas en los fármacos de péptidos cíclicos. Los productos de degradación se producen debido a cambios en el producto farmacéutico almacenado durante mucho tiempo o exposición a la luz, la temperatura, el agua o la reacción a los excipientes. Para garantizar la seguridad y eficacia de los fármacos de péptidos cíclicos, es importante controlar y minimizar las impurezas durante los procesos de síntesis y purificación.
Las impurezas peptídicas generales como la impureza N-Ac, la desamidación en Gln, los residuos de Asn, la desamidación en el extremo C-terminal, la impureza de trisulfuro, el residuo de Cyanoalanice @ Asn, la des-Gly y la endo-Gly de los aminoácidos terminales son comunes en los péptidos cíclicos. también. La degradación y otros péptidos truncados también son una clase importante de impurezas en estos péptidos cíclicos.
Aparte del tipo de impurezas descrito anteriormente, otras impurezas como dímeros paralelos y antiparalelos se forman a menudo en péptidos cíclicos.
- Seq: Cys(1)-Tyr-Phe-Gln-Asn-Cys(6)-Pro-Arg-Gly-CONH2 (enlace de azufre entre cisteínas)
- Dímeros paralelos: 1,1', 6,6'
- Dímeros antiparalelos: 1,6',1',6
- Seq: H-Asn-Asp-Glu-Cys(4)-Glu-Leu-Cys(7)-Val-Asn-Val-Ala-Cys(12)-Thr-Gly-Cys(15)-Leu-OH(4-12), (7-15)-bis(disulfide)
- dímeros paralelos: 4,4', 7,7', 12,12', 15,15';
- dímeros antiparalelos: 4,7',4',7, 12,15', 12',15; o 4,12',4',12,7,15',7',15 o 4,15',4',15, 7,12',7',12
- Seq: H-Cys(1)-Cys(2)-Glu-Tyr-Cys(5)-Cys(6)-Asn-Pro-Ala-Cys(10)-Thr-Gly-Cys(13)-Tyr- OH (3 puentes disulfuro entre 1-6, 2-10 y 5-13 de cisteínas)